RESUME DES CARACTERISTIQUES DU PRODUIT
1. DENOMINATION DU MEDICAMENT
DEPO-ELIGARD 7,5 mg poudre et solvant pour solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Une seringue préremplie de poudre pour solution injectable contient 7,5 mg d'acétate de leuproréline, équivalant à 6,96 mg de leuproréline.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Poudre et solvant pour solution injectable.
Poudre (seringue B) :
Seringue préremplie contenant une poudre blanche à blanc cassé.
Solvant (seringue A) :
Seringue préremplie contenant une solution limpide, incolore à jaune/brun pâle.
4. DONNÉES CLINIQUES
4.1 Indications thérapeutiques
DEPO-ELIGARD 7,5 mg est indiqué dans le traitement du cancer de la prostate hormono-dépendant à un stade avancé et dans le traitement du cancer de la prostate hormono-dépendant localisé à risque élevé et localement avancé en combinaison avec la radiothérapie.
4.2 Posologie et mode d'administration
Posologie
Hommes adultes
DEPO-ELIGARD 7,5 mg doit être administré sous la supervision d'un professionnel de la santé qui dispose de l'expérience appropriée pour surveiller la réponse au traitement.
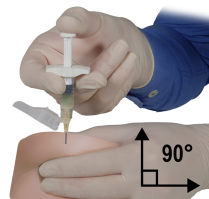
DEPO-ELIGARD 7,5 mg est administré tous les mois en injection sous-cutanée unique. La solution injectée forme un dépôt solide de médicament et assure une libération continue d'acétate de leuproréline pendant un mois.
En règle générale, le traitement du cancer de la prostate avancée par DEPO-ELIGARD 7,5 mg impose un traitement à long terme, lequel ne doit pas être interrompu en cas de rémission ou d'amélioration.
DEPO-ELIGARD 7.5 mg peut être utilisé comme traitement néoadjuvant ou adjuvant en combinaison avec la radiothérapie dans le cancer de la prostate localisé à risque élevé et localement avancé.
La réponse à DEPO-ELIGARD 7,5 mg doit être surveillée en procédant à des examens cliniques et en mesurant les taux sériques de PSA (antigène prostatique spécifique). Les études cliniques ont montré que la testostéronémie augmentait au cours des 3 premiers jours de traitement chez la plupart des patients non orchidectomisés et diminuait ensuite en l'espace de 3 - 4 semaines pour atteindre des valeurs inférieures aux taux de castration médicale.
Une fois atteints, ces taux de castration se maintenaient aussi longtemps que le traitement était poursuivi (< 1 % d'augmentation de la testostéronémie). Si la réponse d'un patient se révèle sous-optimale, il faut s'assurer que la testostéronémie a atteint des taux de castration ou qu'elle se maintient à ces taux. Étant donné qu’un manque d’efficacité peut résulter d’une préparation, reconstitution ou administration incorrecte du produit, les taux de testostérone doivent être évalués si des erreurs de manipulation sont suspectées ou avérées (voir rubrique 4.4).
Chez des patients atteints d’un cancer de la prostate résistant à la castration métastatique, qui n’ont pas été castrés par chirurgie et qui sont traités par un agoniste de la GnRH, tel que la leuproréline, et qui sont éligibles pour un traitement par inhibiteurs de la biosynthèse des androgènes ou par inhibiteurs des récepteurs des androgènes, le traitement par un agoniste de la GnRH peut être poursuivi.
Population pédiatrique
La sécurité et l’efficacité de DEPO-ELIGARD 7,5 mg chez les enfants âgés de 0 à 18 ans n’ont pas été établies (voir également rubrique 4.3).
Populations spécifiques de patients
Aucune étude clinique n'a été réalisée chez les patients atteints d'insuffisance hépatique ou rénale.
Mode d’administration
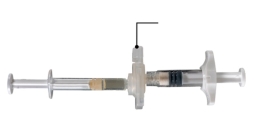
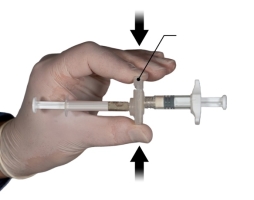
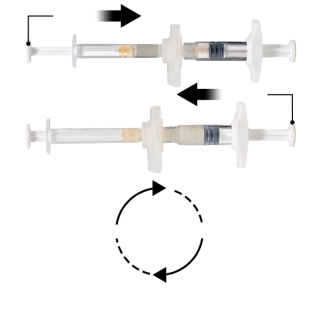
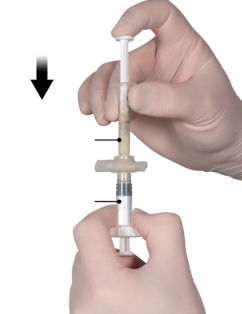
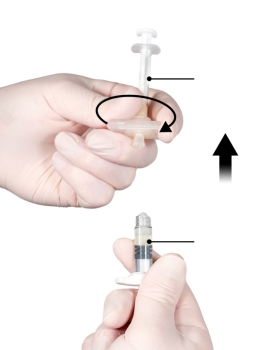
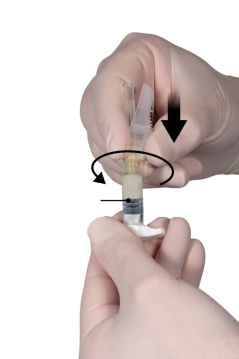
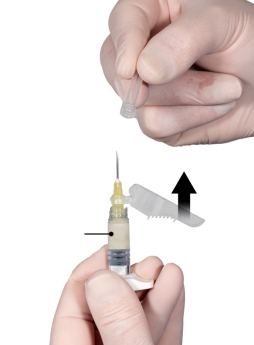
Depo-Eligard 7,5 mg doit être préparé, reconstitué et administré uniquement par des professionnels de la santé habitués à ces procédures. Les instructions de reconstitution et d'administration doivent être strictement respectées (voir rubrique 4.4 et 6.6). Ne pas administrer le produit s’il n’a pas été préparé correctement.
Le contenu de deux seringues stériles préremplies doit être mélangé juste avant l'administration de DEPO-ELIGARD 7,5 mg en injection sous-cutanée.
Au vu des données recueillies dans les expérimentations animales, l'injection intra-artérielle ou intraveineuse doit être absolument évitée.
Comme pour tous les médicaments administrés par voie sous-cutanée, il faut modifier périodiquement le site d'injection.
4.3 Contre-indications
DEPO-ELIGARD 7,5 mg est contre-indiqué chez les femmes et les patients pédiatriques.
Hypersensibilité à l'acétate de leuproréline, aux autres agonistes de la GnRH ou à l’un des excipients mentionnés à la rubrique 6.1.
Patients orchidectomisés (comme avec d'autres agonistes de la GnRH, DEPO-ELIGARD 7,5 mg n'entraîne pas de diminution supplémentaire de la testostéronémie en cas de castration chirurgicale).
Comme traitement unique d'un cancer de la prostate chez les patients souffrant d'une compression médullaire ou de métastases spinales (voir également rubrique 4.4).
4.8 Effets indésirables
Les effets indésirables observés avec DEPO-ELIGARD 7,5 mg sont principalement dus à l'action pharmacologique spécifique de l'acétate de leuproréline, à savoir élévations et diminutions de certaines concentrations hormonales. Les effets indésirables les plus fréquemment rapportés sont les bouffées de chaleur, les nausées, malaise et la fatigue ainsi qu'une irritation locale transitoire au site d'injection. Des bouffées de chaleur légères ou modérées se produisent chez quelque 58 % des patients.
Tableau récapitulatif des effets indésirables
Les événements indésirables suivants ont été rapportés pendant les essais cliniques menés avec DEPO-ELIGARD chez des patients atteints d'un carcinome prostatique avancé. Les événements indésirables sont classés selon les fréquences suivantes : très fréquent (≥ 1/10), fréquent (≥ 1/100, < 1/10), peu fréquent (≥ 1/1,000, < 1/100), rare (≥ 1/10,000, < 1/1,000) et très rare (< 1/10,000), non connu (ne peut être estimé sur la base des données disponibles).
Tableau 1 : Effets indésirables dans les études cliniques menées avec Depo-Eligard | |
Infections et infestations |
|
fréquent | nasopharyngite |
peu fréquent | infection urinaire, infection cutanée locale |
Troubles du métabolisme et de la nutrition |
|
peu fréquent | aggravation d'un diabète |
Affections psychiatriques |
|
peu fréquent | rêves anormaux, dépression, baisse de la libido |
Affections du système nerveux |
|
| |
peu fréquent | vertiges, céphalées, insomnie, trouble du goût, trouble de l'odorat, hypoesthésie, sensation de vertiges |
rare | mouvements involontaires anormaux |
Affections cardiaques | |
Affections vasculaires |
|
très fréquent | bouffées de chaleur |
peu fréquent | hypertension, hypotension |
rare | syncope, collapsus |
Affections respiratoires, thoraciques et médiastinales |
|
peu fréquent | rhinorrhée, dyspnée |
Affections gastro-intestinales |
|
fréquent | nausées, diarrhée, gastro-entérite/colite |
peu fréquent | constipation, sécheresse buccale, dyspepsie, vomissements |
rare | flatulence, éructation |
Affections de la peau et des tissus sous-cutanés |
|
très fréquent | ecchymoses, érythème |
fréquent | prurit, sudation nocturne |
peu fréquent | moiteur, hyperhidrose |
rare | alopécie, éruption cutanée |
Affections musculo-squelettiques et systémiques |
|
fréquent | arthralgie, douleur aux membres, myalgie, raideur, faiblesse |
peu fréquent | dorsalgie, crampes musculaires |
Affections du rein et des voies urinaires |
|
fréquent | mictions rares, difficultés de miction, dysurie, nycturie, oligurie |
peu fréquent | spasmes de la vessie, hématurie, augmentation de la fréquence urinaire, rétention urinaire |
Affections des organes de reproduction et du sein |
|
fréquent | sensibilité mammaire, atrophie testiculaire, douleur dans les testicules, stérilité, hypertrophie mammaire, dysérection, microcaulie, |
peu fréquent | gynécomastie, impuissance, troubles testiculaires |
rare | douleur mammaire |
Troubles généraux et anomalies au site d’administration |
|
très fréquent | fatigue, brûlure au site d'injection, paresthésie au site d'injection |
fréquent | Malaise, douleur au site d'injection, hématome au site d'injection, sensation urticante au site d'injection, |
peu fréquent | prurit au site d'injection, induration au site d’injection, léthargie, douleur, pyrexie |
rare | ulcération au site d'injection |
très rare | nécrose au site d'injection |
|
|
fréquent | modifications hématologiques, anémie |
Investigations |
|
fréquent | augmentation de la créatinine phosphokinase sanguine, augmentation du temps de coagulation |
peu fréquent | augmentation de l'alanine aminotransférase, augmentation des triglycérides sanguins, augmentation du temps de prothrombine, prise de poids |
D'autres événements indésirables qui ont été rapportés en général avec le traitement par l'acétate de leuproréline incluent œdème périphérique, embolie pulmonaire, palpitations, myalgie, faiblesse musculaire, changement dans la sensation de la peau, frissons, éruption cutanée, amnésie et troubles visuels. Une atrophie musculaire a été observée lors de l’utilisation à long terme de produits de cette classe. De rares cas d'apoplexie hypophysaire secondaire à un infarctus ont été rapportés après l'administration d'agonistes de la GnRH de courte et de longue durée d'action. Des cas de thrombocytopénie et de leucopénie ont été rapportés rarement. Des modifications de la tolérance au glucose ont été rapportées.
Des convulsions ont été rapportées après l’administration d’analogues agonistes de la GnRH (voir rubrique 4.4).
Les événements indésirables locaux rapportés après injection de DEPO-ELIGARD 7,5 mg sont semblables à ceux associés aux produits similaires injectés par voie sous-cutanée. Généralement, ces événements indésirables localisés consécutifs à l'injection sous-cutanée sont légers et décrits comme étant de courte durée.
Dans de rares cas, des réactions anaphylactiques/anaphylactoïdes ont été rapportées après l’administration d’analogues agonistes de la GnRH.
Modifications de la densité osseuse
Une diminution de la densité osseuse a été rapportée dans la littérature médicale chez des hommes qui ont subi une orchidectomie ou qui ont été traités par un analogue de la GnRH. Il est probable qu'un traitement à long terme par leuproréline révèle des signes croissants d'ostéoporose. Pour obtenir plus d'informations sur l'augmentation du risque de fracture secondaire à une ostéoporose, voir rubrique 4.4.
Exacerbation des signes et des symptômes de la maladie
Le traitement par leuproréline peut entraîner une exacerbation des signes et des symptômes de la maladie pendant les premières semaines de traitement. Une aggravation d'affections telles que métastases vertébrales et/ou obstruction urinaire ou hématurie peut faire apparaître des problèmes neurologiques tels que faiblesse et/ou paresthésie des membres inférieurs ou une accentuation des symptômes urinaires.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via :
Belgique
Agence Fédérale des Médicaments et des Produits de Santé
www.afmps.be
Division Vigilance :
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy
ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHE
Recordati Industria Chimica e Farmaceutica S.p.A.
Via Matteo Civitali, 1
I-20148 Milano
Italie
8. NUMERO(S) D'AUTORISATION DE MISE SUR LE MARCHE
BE : BE274032
LU : 2005068253
- nat n° 0393118 (1)
- nat n° 0393121 (3)
10. DATE DE MISE A JOUR DU TEXTE
Date d’approbation : 10/2024
| Page 1 de 16 |
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 2224665 | DEPO ELIGARD 7,5 MG PULV SOL INJ 1 | L02AE02 | € 62,74 | - | Oui | € 2 | € 1 |