1. DÉNOMINATION DU MÉDICAMENT
Sandostatine Long Acting Repeatable 20 mg, poudre et solvant pour suspension injectable
Sandostatine Long Acting Repeatable 30 mg, poudre et solvant pour suspension injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un flacon de Sandostatine Long Acting Repeatable, poudre pour suspension injectable contient acétate d’octréotide, correspondant à 20 / 30 mg d’octréotide.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Poudre et solvant pour suspension injectable.
Poudre : poudre blanche à blanc jaunâtre
Solvant pour suspension injectable : solution limpide, incolore à jaune pâle ou brun pâle
4. DONNÉES CLINIQUES
4.1 Indications thérapeutiques
Traitement de l’acromégalie chez les patients pour lesquels la chirurgie est inadaptée ou inefficace, ou pendant la période transitoire précédant la complète efficacité de la radiothérapie (voir rubrique 4.2).
Traitement des patients avec des symptômes associés aux tumeurs endocrines gastro-entéro-pancréatiques fonctionnelles, par exemple les tumeurs carcinoïdes avec signe(s) clinique(s) d'un syndrome carcinoïde (voir rubrique 5.1).
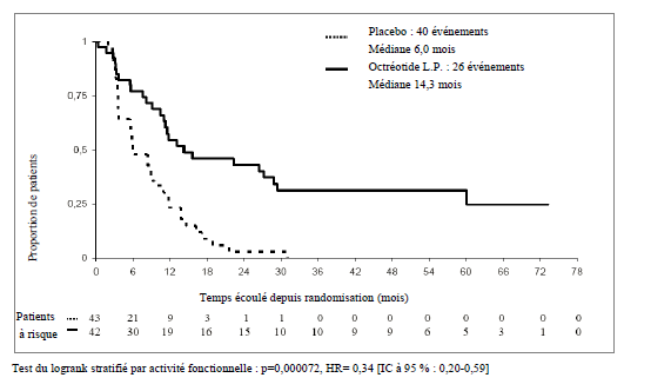
Traitement des patients atteints de tumeurs neuroendocrines avancées de l’intestin moyen ou de localisation primitive inconnue lorsque les sites primitifs ne correspondant pas à l’intestin moyen ont été exclus.
Traitement des adénomes thyréotropes :
- lorsque la sécrétion n’est pas normalisée après chirurgie et/ou radiothérapie ;
- chez les patients ne relevant pas d’un traitement chirurgical ;
- chez les patients irradiés, en attente de l’efficacité de la radiothérapie.
4.2 Posologie et mode d'administration
Posologie
Acromégalie
Il est recommandé de débuter le traitement par Sandostatine Long Acting Repeatable à la posologie de 20 mg toutes les 4 semaines pendant 3 mois. Chez les patients sous traitement par Sandostatine par voie sous-cutanée (s.c.), le traitement avec Sandostatine Long Acting Repeatable peut être initié le lendemain de la dernière administration de Sandostatine s.c. L'ajustement de la dose sera basé sur les taux sériques de l’hormone de croissance (GH) et de l’IGF-1 /Somatomédine C, ainsi que sur les symptômes cliniques.
Si après 3 mois de traitement, les symptômes cliniques et les taux hormonaux (GH ; IGF-1) ne sont pas complètement contrôlés (concentration de GH toujours > 2,5 microgrammes/L), la dose de Sandostatine Long Acting Repeatable peut être augmentée à 30 mg administrée toutes les 4 semaines. Si trois mois plus tard, les concentrations de GH et d’IGF-1 sont insuffisamment contrôlées par l'administration de 30 mg de Sandostatine Long Acting Repeatable, la dose pourra être augmentée à 40 mg toutes les 4 semaines.
Chez les patients dont le taux de GH se maintient, toujours, au-dessous de 1 microgramme/L, dont le taux d’IGF-1 est normalisé et chez qui les principaux signes/symptômes réversibles de l'acromégalie ont disparu après 3 mois de traitement à la dose de 20 mg, il est possible de réduire la dose à 10 mg de Sandostatine Long Acting Repeatable toutes les 4 semaines. Néanmoins, chez ces patients qui reçoivent de faibles doses de Sandostatine Long Acting Repeatable, une surveillance stricte des valeurs sériques de GH et d’IGF-1 et de l'évolution clinique est recommandée.
Pour les patients qui sont traités par une dose stable de Sandostatine Long Acting Repeatable, un dosage des taux de GH et d'IGF-1 doit être réalisé tous les 6 mois.
Tumeurs endocrines gastro-entéro-pancréatiques
Traitement des patients présentant des symptômes associés aux tumeurs neuroendocrines gastro-entéro-pancréatiques fonctionnelles
Il est recommandé de débuter le traitement par Sandostatine Long Acting Repeatable à la posologie de 20 mg toutes les 4 semaines. Chez les patients sous traitement par Sandostatine par voie sous-cutanée (s.c.), l’administration de Sandostatine (s.c.) doit être poursuivie, pendant les 2 semaines qui suivent la première injection de Sandostatine Long Acting Repeatable à la même posologie efficace que précédemment.
Chez les patients dont les symptômes et les marqueurs biologiques sont bien contrôlés après 3 mois de traitement, la posologie peut être réduite à 10 mg de Sandostatine Long Acting Repeatable toutes les 4 semaines.
Chez les patients dont les symptômes ne sont que partiellement contrôlés après 3 mois de traitement, la posologie peut être augmentée à 30 mg de Sandostatine Long Acting Repeatable toutes les 4 semaines.
Durant les périodes où les symptômes liés aux tumeurs neuroendocrines gastro-entéro-pancréatiques pourraient se majorer pendant le traitement par Sandostatine Long Acting Repeatable, il est recommandé d’administrer simultanément Sandostatine par voie sous-cutanée à la dose qui était pratiquée avant l’instauration du traitement par Sandostatine Long Acting Repeatable. Cela peut se produire principalement au cours des 2 premiers mois de traitement car les concentrations thérapeutiques efficaces d’octréotide n’ont pas encore été atteintes.
Traitement des patients atteints de tumeurs neuroendocrines avancées de l’intestin moyen ou de localisation primitive inconnue lorsque les sites primitifs ne correspondant pas à l’intestin moyen ont été exclus.
La dose recommandée de Sandostatine Long Acting Repeatable est de 30 mg toutes les 4 semaines (voir rubrique 5.1). Le traitement par Sandostatine Long Acting Repeatable dans le but de contrôler la tumeur doit être poursuivi en l’absence de progression tumorale.
Adénomes thyréotropes
Le traitement par Sandostatine Long Acting Repeatable doit débuter à la posologie de 20 mg toutes les 4 semaines pendant 3 mois avant d'envisager une adaptation posologique. La dose sera adaptée en fonction de la réponse de la TSH et des hormones thyroïdiennes.
Insuffisance rénale
L’insuffisance rénale n’a pas modifié l’aire sous la courbe (ASC) de l’octréotide injecté par voie sous-cutané. Il n’est donc pas nécessaire d'ajuster la dose de Sandostatine Long Acting Repeatable.
Insuffisance hépatique
Lors d’une étude réalisée avec Sandostatine administrée par voie sous-cutanée et par voie intraveineuse, il a été montré que la capacité d’élimination pouvait être réduite chez les patients atteints de cirrhose, mais pas chez les patients atteints de stéatose hépatique. Dans certains cas, un ajustement de la dose pourrait être nécessaire chez des patients présentant une insuffisance hépatique.
Population âgée
Dans une étude réalisée avec Sandostatine administrée par voie sous-cutanée aucun ajustement de la dose n’a été nécessaire chez des sujets âgés de 65 ans et plus. Ainsi, il n’est pas nécessaire d’adapter la dose chez ces patients.
Population pédiatrique
Les données relatives à l'utilisation de Sandostatine Long Acting Repeatable chez l’enfant sont limitées.
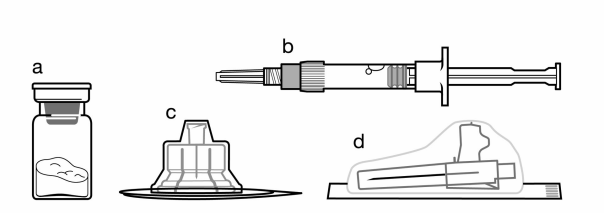
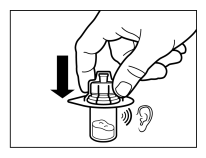
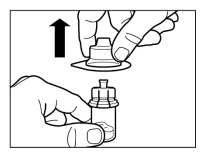
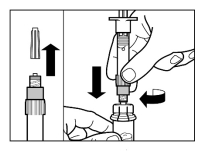
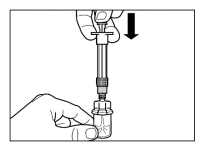
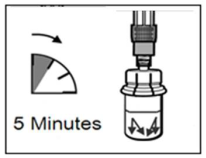
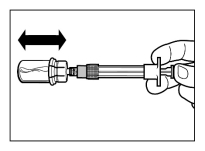
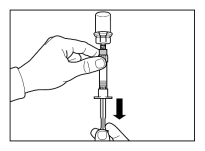
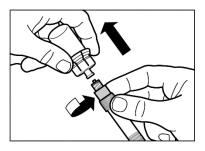
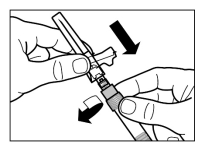
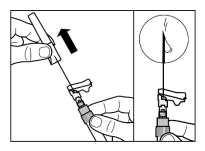
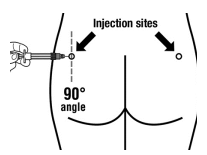
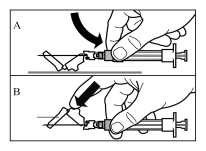
Mode d’administration
Sandostatine Long Acting Repeatable doit être exclusivement administrée par injection intramusculaire profonde. En cas d'administrations intramusculaires répétées, les injections doivent être effectuées alternativement dans le muscle fessier droit et gauche (voir rubrique 6.6).
4.3 Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.8 Effets indésirables
Synthèse du profil de sécurité
Les effets indésirables les plus fréquemment rapportés avec l’octréotide sont des troubles gastro-intestinaux, des troubles du système nerveux, des troubles hépato-biliaires, et des troubles nutritionnels et du métabolisme.
Les effets indésirables les plus fréquemment rapportés dans les études cliniques avec l'octréotide étaient : diarrhées, douleurs abdominales, nausées, flatulences, céphalées, cholélithiase, hyperglycémie et constipation. D'autres effets indésirables ont été fréquemment rapportés comme des sensations vertigineuses, des douleurs localisées, des boues biliaires, des dysfonctionnements thyroïdiens (par ex. diminution de la TSH, diminution de la T4 totale et diminution de la T4 libre), des selles molles, une intolérance au glucose, des vomissements, une asthénie et une hypoglycémie.
Liste tabulée des effets indésirables
Les effets indésirables listés dans le Tableau 1, ci-dessous ont été rapportés lors des études cliniques avec l’octréotide :
Les effets indésirables (Tableau 1) sont classés par ordre décroissant de fréquence selon la convention suivante : très fréquent (1/10), fréquent (1/100, <1/10), peu fréquent (1/1.000, <1/100), rare (1/10.000, <1/1.000) et très rare (<1/10.000), incluant les cas isolés. Au sein de chaque catégorie de fréquence, les effets indésirables sont présentés par ordre décroissant de gravité.
Tableau 1 Effets indésirables rapportés au cours des essais cliniques
Affections gastro-intestinales | |
Très fréquent: | Diarrhée, douleurs abdominales, nausées, constipation, flatulences |
Affections du système nerveux | |
Très fréquent: | Céphalées |
Affections endocriniennes | |
Fréquent: | Hypothyroïdie, trouble thyroïdien (par ex. : diminution de la TSH, diminution de la T4 totale et diminution de la T4 libre) |
Affections hépatobiliaires | |
Très fréquent: | Cholélithiase |
Troubles du métabolisme et de la nutrition | |
Très fréquent: | Hyperglycémie |
Troubles généraux et anomalies au site d’administration | |
Très fréquent: | Réactions au site d’injection |
Fréquent : | Asthénie |
Investigations | |
Fréquent: | Augmentation des transaminases |
Affections de la peau et du tissu sous–cutané | |
Fréquent: | Prurit, rash, alopécie |
Affections respiratoires, thoraciques et médiastinales | |
Fréquent: | Dyspnée |
Affections cardiaques | |
Fréquent: | Bradycardie |
Post-commercialisation
Les effets indésirables listés dans le Tableau 2 ont été rapportés spontanément et il n’est pas toujours possible d’évaluer leur fréquence ou la relation de cause à effet avec l’exposition au médicament.
Tableau 2 Effets indésirables issus de la notification spontanée
Affections hématologiques et du système lymphatique |
Affections du système immunitaire |
Affections de la peau et du tissu sous–cutané |
Affections hépatobiliaires |
Affections cardiaques |
Investigations |
Description de certains effets indésirables
Réactions de la vésicule biliaire et associées
Il a été démontré que les analogues de la somatostatine inhibent la contractilité de la vésicule biliaire et diminuent la sécrétion biliaire, ce qui peut entraîner des anomalies de la vésicule biliaire ou de la boue biliaire. L’incidence de la formation de calculs biliaires sous traitement au long cours par Sandostatine s.c. est estimée à environ 15 à 30 %. La prévalence dans la population générale (entre 40 et 60 ans) est environ de 5 à 20 %. Un traitement par Sandostatine Long Acting Repeatable au long cours, comparé à la forme s.c, n’augmente pas l’incidence des lithiases vésiculaires chez des patients acromégales ou atteints de tumeurs neuroendocrines gastro-entéro-pancréatiques. Les calculs sont généralement asymptomatiques ; les calculs symptomatiques doivent être traités soit par dissolution par des acides biliaires, soit par chirurgie.
Affections gastro-intestinales
Dans de rares cas, les effets indésirables gastro-intestinaux peuvent évoquer une occlusion intestinale aiguë avec distension abdominale progressive, douleur épigastrique sévère, sensibilité et défense abdominales.
En général, la fréquence des événements gastro-intestinaux décroît progressivement au cours du traitement.
Réactions d’hypersensibilité et anaphylactiques
Des réactions d’hypersensibilité et anaphylactiques ont été rapportées au cours de la post-commercialisation. Celles-ci touchent principalement la peau, rarement la bouche et les voies respiratoires. Des cas isolés de choc anaphylactique ont été rapportés.
Réactions au site d'injection
Des réactions au site d'injection, notamment douleur, rougeur, hémorragie, prurit, oedème ou induration ont été fréquemment rapportées chez les patients recevant un traitement par Sandostatine Long Acting Repeatable. Cependant, ces événements n'ont pas nécessité d’intervention médicale dans la majorité des cas.
Troubles du métabolisme et de la nutrition
Bien que l’excrétion de graisses dans les selles puisse être augmentée, il n’y a pas de preuve à ce jour que le traitement au long cours par l’octréotide puisse conduire à une carence nutritionnelle par malabsorption.
Enzymes pancréatiques
Dans de très rares cas, des pancréatites aiguës ont été rapportées dans les premières heures ou les premiers jours du traitement par Sandostatine s.c., et se sont résolues à l’arrêt du traitement. Par ailleurs, des cas de pancréatites dues à une lithiase biliaire ont été rapportés chez des patients traités au long cours par Sandostatine s.c..
Affections cardiaques
La bradycardie est un effet indésirable fréquent des analogues de la somatostatine. Chez des patients atteints d’acromégalie ou de syndromes carcinoïdes, des modifications de l’ECG telles que : allongement de l’intervalle QT, déviation axiale, repolarisation précoce, microvoltage, transition R/S, onde R précoce et modifications non spécifiques du segment ST-T ont été observés. La relation entre ces événements et le traitement par acétate d’octréotide n’a cependant pas été établie car de nombreux patients présentaient des pathologies cardiaques associées (voir rubrique 4.4).
Thrombocytopénie
La thrombocytopénie a été rapportée au cours de la post-commercialisation, en particulier pendant le traitement par Sandostatine administrée par voie intraveineuse chez des patients souffrant d’une cirrhose du foie et pendant le traitement par Sandostatine Long Acting Repeatable. Cet effet indésirable est réversible après l’arrêt du traitement.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via:
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance :
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Novartis Pharma SA
Medialaan 40
B-1800 Vilvoorde
8. NUMEROS D’AUTORISATION DE MISE SUR LE MARCHE
Sandostatine Long Acting Repeatable 20 mg: BE191737 / LU: 1998020007
- 0755153: 1*1 flacon poudre + 1*1 seringue prer. solvant
Sandostatine Long Acting Repeatable 30 mg: BE191685 / LU: 1998020011
- 0755167: 1*1 flacon poudre + 1*1 seringue prer. solvant
10. DATE DE MISE A JOUR DU TEXTE
02/2026
Date d’approbation: 05/2026
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 1395052 | SANDOSTATINE LAR 1FL 30MG | H01CB02 | € 754,27 | - | Oui | € 12,8 | € 8,5 |
| 1395060 | SANDOSTATINE LAR 1FL 20MG | H01CB02 | € 561,56 | - | Oui | € 12,8 | € 8,5 |