RESUME DES CARACTERISTIQUES DU PRODUIT
1. DENOMINATION DU MEDICAMENT
Minulet 0,075 mg/0,030 mg comprimés enrobés
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé contient 0,075 mg de gestodène et 0,030 mg d'éthinylestradiol.
Excipients à effet notoire : lactose et saccharose (chaque comprimé contient 37,43 mg de lactose monohydraté et 19,66 mg de saccharose; voir rubrique 4.4).
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Comprimés enrobés
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Contraception hormonale orale
La décision de prescrire Minulet doit être prise en tenant compte des facteurs de risque de la patiente, notamment ses facteurs de risque de thrombo-embolie veineuse (TEV), ainsi que du risque de TEV associé à Minulet en comparaison aux autres CHC (Contraceptifs Hormonaux Combinés) (voir rubriques 4.3 et 4.4).
4.2 Posologie et mode d’administration
Ne pas commencer ni continuer la prise de Minulet en cas de suspicion ou présence de grossesse.
Posologie
Comment prendre Minulet
Les comprimés doivent être pris dans l’ordre indiqué sur la plaquette, tous les jours environ à la même heure, pendant 21 jours consécutifs avec un arrêt de 7 jours entre chaque plaquette. Une hémorragie de privation débute habituellement 2 à 3 jours après la prise du dernier comprimé et peut se poursuivre après le début de la plaquette suivante.
Comment débuter Minulet
Absence de contraception hormonale au cours du mois précédent
L’utilisatrice doit commencer à prendre Minulet le premier jour de son cycle menstruel (càd le premier jour des règles).
Commencer Minulet entre le 2ème et le 7ème jour du cycle menstruel est permis ; néanmoins, l’utilisation d’une méthode complémentaire de contraception non-hormonale de type mécanique (préservatifs, spermicides…) pendant les 7 premiers jours de Minulet est recommandée.
En relais d’un autre contraceptif hormonal combiné (CHC) oral
L’utilisation de Minulet devrait commencer le jour suivant la prise du dernier comprimé actif du CHC oral précédent mais, au plus tard, le jour suivant la période habituelle sans comprimés ou le dernier comprimé inactif du CHC oral précédent.
En relais d’un contraceptif progestatif (pilule, injectable, dispositif intra utérin, implant)
L’utilisatrice peut arrêter l’utilisation d’une pilule progestative (minipilule) n’importe quel jour ; l’utilisation de Minulet doit commencer le lendemain. L’utilisation de Minulet doit se faire le jour du retrait d’un implant ou d’un dispositif intra utérin. L’utilisation de Minulet doit se faire le jour prévu pour la prochaine injection progestative.
Dans tous ces cas, il est recommandé à l’utilisatrice d'utiliser une méthode complémentaire de contraception non-hormonale de type mécanique (préservatifs, spermicides…) pendant les 7 premiers jours de la prise de Minulet.
Après une interruption de grossesse du premier trimestre
L’utilisatrice peut débuter Minulet immédiatement. Dans ce cas, aucune méthode complémentaire de contraception n’est nécessaire.
Postpartum
L’augmentation du risque de thrombo-embolie pendant la grossesse, et en particulier pendant les 6 semaines de la période puerpérale, doit être prise en compte (voir rubrique 4.4 – Facteurs de risque de TEV).
Minulet ne peut être débuté qu’à partir du 28ème jour après un accouchement (pour les utilisatrices qui choisissent de ne pas allaiter) ou après une interruption de grossesse du deuxième trimestre. Il est recommandé d’utiliser une méthode complémentaire de contraception non-hormonale de type mécanique (préservatifs, spermicides…) pendant les 7 premiers jours de la prise de Minulet. Une grossesse doit être exclue lorsque des rapports sexuels ont eu lieu avant l’instauration de Minulet ; sinon, la femme doit attendre son premier cycle menstruel avant de commencer Minulet.
Pour les femmes qui allaitent, se reporter à la rubrique 4.6.
Que faire en cas d’oubli de comprimés
La protection contraceptive peut être diminuée en cas d’oubli de comprimés de Minulet, particulièrement si cet oubli augmente l’intervalle de temps entre le dernier comprimé de la plaquette en cours et le premier comprimé de la plaquette suivante.
- Si l’oubli d’un comprimé est constaté dans les 12 heures qui suivent l’heure habituelle de la prise, prendre immédiatement le comprimé oublié et poursuivre le traitement en prenant le comprimé suivant à l’heure habituelle.
- Si l’oubli d’un comprimé est constaté plus de 12 heures après l’heure habituelle de la prise ou si plus d’un comprimé a été oublié, la protection contraceptive n’est plus garantie.
o Prendre immédiatement le comprimé oublié, ce qui peut résulter en deux comprimés qui doivent être pris le même jour, et poursuivre le traitement en prenant le comprimé suivant à l’heure habituelle, en utilisant simultanément une méthode complémentaire de contraception non-hormonale de type mécanique (préservatifs, spermicides…) pendant les 7 jours suivants.
- Si cette période de sécurité de 7 jours avec préservatif s’étend au-delà du dernier comprimé de la plaquette en cours, supprimer la pause entre les deux plaquettes et démarrer la plaquette suivante immédiatement après la prise du dernier comprimé. Une période sans prise de comprimés entre 2 plaquettes n’est pas permise. Ceci évite une période trop longue sans prise de comprimés et réduit le risque d’une ovulation non-voulue. Il est probable qu’aucune hémorragie de privation ne survienne avant la fin de la nouvelle plaquette. L’utilisatrice peut cependant présenter du spotting ou des hémorragies intercurrentes.
- S’il ne se produit pas d’hémorragie de privation à la fin de la nouvelle plaquette, la possibilité d’une grossesse doit être exclue avant d’entamer une nouvelle plaquette.
Que faire en cas de vomissements et/ou diarrhée
Si des vomissements ou une diarrhée se produisent dans les 4 heures qui suivent la prise d’un comprimé, l’absorption des comprimés peut être réduite. Dans ces cas, les instructions concernant l’oubli de comprimés doivent être suivies (cfr oubli de moins de 12h) et l’utilisatrice prendra un comprimé d’une plaquette de réserve. Si l’utilisatrice ne possède plus de plaquette de réserve, une méthode complémentaire de contraception non-hormonale s'impose pendant le reste du cycle. Il faut cependant continuer à prendre les comprimés de la plaquette entamée afin d'éviter une hémorragie de privation précoce. D'autres méthodes contraceptives (de type mécanique comme le préservatif, les spermicides…) doivent être envisagées si l'on s'attend à ce que les troubles gastro-intestinaux persistent.
Population pédiatrique
L’efficacité et la sécurité des CHC oraux ont été démontrées chez les femmes en âge de reproduire. Ces produits ne doivent pas être utilisés avant l’apparition des premières règles.
Utilisation gériatrique
Les CHC oraux ne sont pas indiqués chez les femmes postménopausées.
Mode d’administration
Voie orale.
4.3 Contre-indications
Les CHC oraux ne peuvent pas être utilisés en présence d’une des conditions citées ci-après. L’utilisation de Minulet doit être immédiatement interrompue si l’une des conditions suivantes apparaît pour la première fois.
- Présence ou risque de thrombo-embolie artérielle (TEA)
- Thrombo-embolie artérielle – présence ou antécédents de thrombo-embolie artérielle (p. ex. infarctus du myocarde [IM]) ou de prodromes (p. ex. angine de poitrine)
- Affection cérébrovasculaire – présence ou antécédents d’accident vasculaire cérébral (AVC) ou de prodromes (p. ex. accident ischémique transitoire [AIT])
- Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie artérielle, telle qu’une hyperhomocystéinémie ou la présence d’anticorps anti-phospholipides (anticorps anti-cardiolipine, anticoagulant lupique).
- Antécédents de migraine avec signes neurologiques focaux
- Risque élevé de thrombo-embolie artérielle dû à la présence de multiples facteurs de risque (voir rubrique 4.4) ou d’un facteur de risque sévère tel que :
- diabète avec symptômes vasculaires (micro ou macro angiopathie)
- hypertension artérielle sévère
- dyslipoprotéinémie sévère
- Maladie coronarienne;
- Présence ou risque de thrombo-embolie veineuse (TEV)
- Thrombo-embolie veineuse – présence de TEV (patient traité par des anticoagulants) ou antécédents de TEV (p. ex. thrombose veineuse profonde [TVP] ou embolie pulmonaire [EP])
- Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie veineuse, telle qu’une résistance à la protéine C activée (PCa) (y compris une mutation du facteur V de Leiden), un déficit en antithrombine III, un déficit en protéine C, un déficit en protéine S
- Intervention chirurgicale majeure avec immobilisation prolongée (voir rubrique 4.4)
- Risque élevé de thrombo-embolie veineuse dû à la présence de multiples facteurs de risque (voir rubrique 4.4);
- Valvulopathie thrombogène;
- Troubles du rythme thrombogène;
- Suspicion ou présence de carcinome mammaire;
- Suspicion ou présence d’affections néoplasiques estrogéno-sensibles (endomètre...);
- Adénomes ou carcinomes hépatiques;
- Affections hépatiques sévères jusqu’au retour à la normale de la fonction hépatique;
- Hémorragies vaginales non diagnostiquées;
- Suspicion ou présence de grossesse;
- Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1 ;
- Présence ou antécédents de pancréatite associée à une hypertriglycéridémie sévère.
Minulet est contre-indiqué en administration concomitante avec des médicaments contenant l’association ombitasvir/paritaprévir/ritonavir, et le dasabuvir, ou de médicament contenant glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprévir (voir rubrique 4.5).
4.8 Effets indésirables
Description de certains effets indésirables particuliers
Une augmentation du risque d'événement thrombotique et thrombo-embolique artériel et veineux, incluant l’infarctus du myocarde, l’AVC, les accidents ischémiques transitoires, la thrombose veineuse et l’embolie pulmonaire, a été observée chez les femmes utilisant des CHC ; ceci est abordé plus en détails en rubrique 4.4.
L’utilisation de CHC oraux est également associé à un risque accru de:
- néoplasie cervicale intra-épithéliale et de cancer cervical ;
- diagnose d’un cancer mammaire.
- tumeurs hépatiques bénignes (p. ex. hyperplasie focale nodulaire, adénome hépatique)
Voir aussi rubrique 4.4.
Les effets indésirables suivants sont listés par catégorie de fréquence comme suit :
Très fréquent ≥1/10
Fréquent ≥1/100,<1/10
Peu fréquent 1/1 000, <1/100
Rare 1/10 000, <1/1 000
Très rare <1/10 000
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
Système/organe cible | Effet indésirable |
Infections et infestations |
|
Fréquent | Vaginite incluant la candidose vaginale |
Tumeurs bénignes, malignes et non précisées (incl kystes et polypes) | |
Affections du système immunitaire | |
Rare | |
Troubles du métabolisme et de la nutrition |
|
Peu fréquent | Augmentation ou diminution de l’appétit |
Rare | Intolérance au glucose |
Très rare | Exacerbation d’une porphyrie |
Affections psychiatriques |
|
Fréquent | Modifications de l’humeur et de la libido, dépression |
Affections du système nerveux | |
Très fréquent | Maux de tête, migraine |
Fréquent | Nervosité, vertiges |
Très rare | Exacerbation d’une chorée |
Affections oculaires | |
Affections vasculaires | |
Affections gastro-intestinales | |
Affections hépatobiliaires | |
Affections de la peau et du tissu sous-cutané | |
Affections du rein et des voies urinaires | |
Affections des organes de reproduction et du sein | |
Troubles généraux et anomalies au site d’administration | |
Investigations | |
* La névrite optique peut provoquer une cécité partielle ou totale.
** Les CHC oraux peuvent exacerber une affection de la vésicule biliaire existante ou peut activer le développement d’une telle affection chez les utilisatrices asymptomatiques.
*** Les taux sériques en folates peuvent être diminués sous CHC oraux. Ceci peut être de signification clinique si l’utilisatrice tombe enceinte rapidement après l’arrêt de la pilule.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via :
Belgique : l’Agence fédérale des médicaments et des produits de santé
www.afmps.be - Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e mail: adr@fagg-afmps.be
Luxembourg : Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santéSite internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Pfizer NV/SA
Boulevard de la Plaine 17
1050 Bruxelles
8. NUMERO D’AUTORISATION DE MISE SUR LE MARCHE
BE142502; 2006109087
10. DATE DE MISE A JOUR DU TEXTE
03/2025
25B17
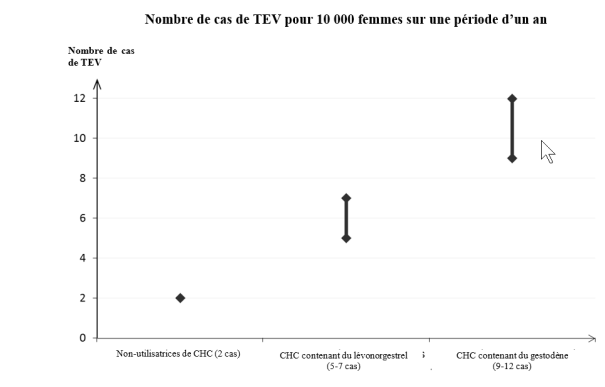
[1] Ces incidences ont été estimées à partir de l’ensemble des données des études épidémiologiques, en s’appuyant sur les risques relatifs liés aux différents CHC en comparaison aux CHC contenant du lévonorgestrel.
[2] Point central de l’intervalle de 5-7 pour 10 000 années-femmes sur la base d’un risque relatif, pour les CHC contenant du lévonorgestrel par rapport à la non-utilisation d’un CHC, d’environ 2,3 à 3,6
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 0662502 | MINULET DRAG 3 X 21 | G03AA10 | € 15,42 | - | Oui | € 6,42 | € 6,42 |