ANNEXE I
RESUME DES CARACTERISTIQUES DU PRODUIT
1. DENOMINATION DU MEDICAMENT
Bavencio 20 mg/mL solution à diluer pour perfusion
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque mL de solution à diluer contient 20 mg d’avélumab.
Un flacon de 10 mL contient 200 mg d’avélumab.
Avélumab est un anticorps monoclonal IgG1 humain dirigé contre la protéine de surface immunomodulatrice PD‑L1, ligand du récepteur PD‑1. Il est produit dans des cellules ovariennes de hamster chinois par la technique de l’ADN recombinant.
Excipients à effet notoire
Ce médicament contient 5 mg de polysorbate 20 par flacon.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Solution à diluer pour perfusion (solution à diluer stérile).
Solution limpide, incolore à légèrement jaune. Le pH de la solution est compris entre 5,0 et 5,6 et son osmolalité se situe entre 285 et 350 mOsm/kg.
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Bavencio est indiqué en monothérapie pour le traitement de patients atteints de carcinome à cellules de Merkel (CCM) métastatique de l’adulte.
Bavencio est indiqué en monothérapie pour le traitement d’entretien de première ligne des patients adultes atteints de carcinome urothélial (CU) à un stade localement avancé ou métastatique, dont la maladie n’a pas progressé après la chimiothérapie à base de sel de platine.
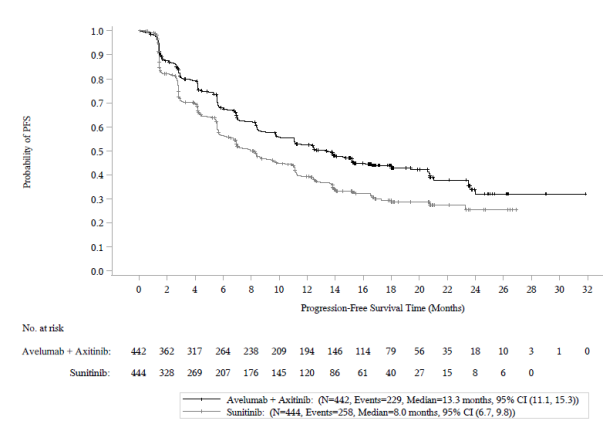
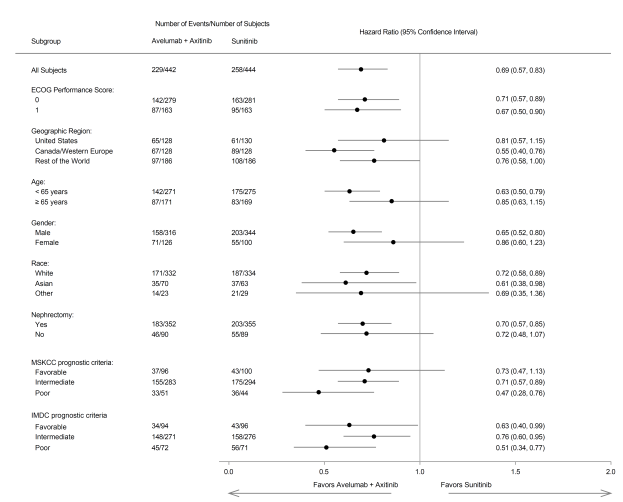
Bavencio, en association avec axitinib, est indiqué dans le traitement de première ligne des patients adultes atteints de carcinome à cellules rénales (CCR) à un stade avancé (voir rubrique 5.1).
4.2 Posologie et mode d’administration
Le traitement doit être instauré et supervisé par un médecin expérimenté en matière de traitement du cancer.
Posologie
La dose recommandée de Bavencio en monothérapie est de 800 mg à administrer par voie intraveineuse pendant 60 minutes toutes les 2 semaines.
L’administration de Bavencio doit être poursuivie selon le schéma recommandé jusqu’à la progression de la maladie ou l’apparition d’une toxicité inacceptable.
La dose recommandée de Bavencio en association avec axitinib est de 800 mg à administrer par voie intraveineuse pendant 60 minutes toutes les 2 semaines, avec la prise concomitante de 5 mg d’axitinib à prendre par voie orale deux fois par jour (à 12 heures d’intervalle) avec ou sans nourriture jusqu’à la progression de la maladie ou l’apparition d’une toxicité inacceptable.
Pour toute information relative à la posologie d’axitinib, veuillez vous reporter aux informations sur le produit axitinib.
Prémédication
Les patients doivent recevoir une prémédication composée d’un antihistaminique et de paracétamol avant les 4 premières perfusions de Bavencio. Si la quatrième perfusion a pu être réalisée sans que survienne de réaction liée à la perfusion, l’administration de la prémédication avant les doses suivantes sera laissée à l’appréciation du médecin.
Modifications du traitement
Les augmentations ou réductions de dose ne sont pas recommandées. Un report ou une interruption du traitement peuvent être nécessaires au cas par cas en fonction de la sécurité d’emploi et de la tolérance ; voir le Tableau 1.
Les recommandations précises pour la prise en charge des effets indésirables à médiation immunitaire sont présentées dans la rubrique 4.4.
Tableau 1 : Recommandations pour la suspension ou l’arrêt de Bavencio
Effet indésirable lié au traitement | Sévérité* | Modification du traitement |
Réaction liée à la perfusion | Réaction liée à la perfusion de grade 1 | Réduire le débit de perfusion de 50 % |
Réaction liée à la perfusion de grade 2 | Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 ; reprendre la perfusion à un débit réduit de 50 % | |
Réaction liée à la perfusion de grade 3 ou de grade 4 | Arrêter définitivement le traitement | |
Pneumopathie | Pneumopathie de grade 2 | Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 |
Pneumopathie de grade 3 ou de grade 4, ou pneumopathie récurrente de grade 2 | Arrêter définitivement le traitement | |
Hépatite | Aspartate aminotransférases (ASAT) ou alanine aminotransférases (ALAT) supérieures à 3 fois et inférieures ou égales à 5 fois la limite normale supérieure (LNS) ou bilirubine totale supérieure à 1,5 fois et inférieure ou égale à 3 fois la LNS | Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 |
ASAT ou ALAT supérieures à 5 fois la LNS ou bilirubine totale supérieure à 3 fois la LNS | Arrêter définitivement le traitement | |
Colite | Colite ou diarrhée de grade 2 ou de grade 3 | Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 |
Colite ou diarrhée de grade 4 ou colite récurrente de grade 3 | Arrêter définitivement le traitement | |
Pancréatite | Pancréatite suspectée | Suspendre le traitement |
Pancréatite confirmée | Arrêter définitivement le traitement | |
Myocardite | Myocardite suspectée | Suspendre le traitement |
Myocardite confirmée | Arrêter définitivement le traitement | |
Endocrinopathies (hypothyroïdie, hyperthyroïdie, insuffisance surrénalienne, hyperglycémie) | Endocrinopathies de grade 3 ou de grade 4 | Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 |
Néphrite et dysfonction rénale | Taux de créatinine sérique compris entre 1,5 fois et 6 fois la LNS | Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 |
Taux de créatinine sérique supérieur à 6 fois la LNS | Arrêter définitivement le traitement | |
Réactions cutanées | Éruption cutanée de grade 3 | Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 |
Éruption cutanée de grade 4 ou récurrente de grade 3 ou syndrome de Stevens‑Johnson (SSJ) ou nécrolyse épidermique toxique (NET) confirmés | Arrêter définitivement le traitement | |
Autres effets indésirables à médiation immunitaire (dont les autres effets indésirables à médiation immunitaire cliniquement importants mentionnés au paragraphe « Autres effets indésirables à médiation immunitaire » [voir rubrique 4.4]) | Pour les effets suivants :
| Suspendre le traitement jusqu’à régression des effets indésirables à un grade 0‑1 |
Pour les effets suivants :
| Arrêter définitivement le traitement |
* Toxicité évaluée selon les Critères Communs de Terminologie pour les Effets Indésirables du National Cancer Institute, version 4.0 (NCI‑CTCAE v4.03)
Modifications du traitement lorsque Bavencio est utilisé en association avec axitinib
Si le taux d’ALAT ou d’ASAT est ≥ 3 fois la LNS mais < 5 fois la LNS ou si la bilirubine totale est ≥ 1,5 fois la LNS mais < 3 fois la LNS, Bavencio et axitinib doivent tous deux être suspendus jusqu’à ce que ces effets indésirables régressent à un grade 0‑1. S’ils persistent (plus de 5 jours), une corticothérapie par prednisone ou un équivalent, suivie d’une réduction progressive, doit être envisagée. Après rétablissement, une reprise du traitement par Bavencio ou axitinib, ou une reprise séquentielle par Bavencio et axitinib doit être envisagée. Une réduction de la dose selon les informations sur le produit axitinib doit être envisagée en cas de reprise du traitement par axitinib.
Si le taux d’ALAT ou d’ASAT est ≥ 5 fois la LNS ou > 3 fois la LNS avec en parallèle un taux de bilirubine totale ≥ 2 fois la LNS, ou si le taux de bilirubine totale est ≥ 3 fois la LNS, Bavencio et axitinib doivent tous deux être arrêtés définitivement et une corticothérapie doit être envisagée.
Conseils concernant la modification de la dose d’axitinib lorsqu’il est utilisé avec Bavencio
Lorsque Bavencio est administré en association avec axitinib, veuillez vous reporter aux informations sur le produit axitinib pour connaître les modifications de dose recommandées pour axitinib.
Populations particulières
Personnes âgées
Aucun ajustement posologique n’est nécessaire chez les patients âgés (≥ 65 ans) (voir rubriques 5.1 et 5.2).
Insuffisance rénale
Aucun ajustement posologique n’est nécessaire chez les patients atteints d’insuffisance rénale légère ou modérée (voir rubrique 5.2). Les données concernant les patients atteints d’insuffisance rénale sévère sont insuffisantes pour donner des recommandations posologiques.
Insuffisance hépatique
Aucun ajustement posologique n’est nécessaire chez les patients atteints d’insuffisance hépatique légère (voir rubrique 5.2). Les données concernant les patients atteints d’insuffisance hépatique modérée ou sévère sont insuffisantes pour donner des recommandations posologiques.
Population pédiatrique
La sécurité et l’efficacité de Bavencio chez les enfants et les adolescents âgés de moins de 18 ans n’ont pas été établies. Les données actuellement disponibles concernant Bavencio sont décrites à la rubrique 5.1 mais aucune recommandation sur la posologie ne peut être donnée.
Mode d’administration
Bavencio est destiné à être utilisé en perfusion intraveineuse exclusivement. Il ne doit pas être administré en injection intraveineuse rapide ni en bolus intraveineux.
Bavencio doit être dilué dans une solution pour perfusion de chlorure de sodium à 9 mg/mL (0,9 %) ou une solution pour perfusion de chlorure de sodium à 4,5 mg/mL (0,45 %). Il sera ensuite administré en perfusion intraveineuse pendant 60 minutes en utilisant un filtre intégré ou additionnel stérile, apyrogène, à faible liaison aux protéines, de 0,2 micromètre.
Pour les instructions concernant la préparation et l’administration du médicament, voir la rubrique 6.6.
4.3 Contre‑indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.8 Effets indésirables
Résumé du profil de sécurité
Avélumab est associé à des effets indésirables à médiation immunitaire. La plupart d’entre eux, y compris les réactions sévères, se sont résolus après instauration d’un traitement médical approprié ou arrêt d’avélumab (voir « Description de certains effets indésirables particuliers » ci‑dessous).
Les effets indésirables les plus fréquents avec avélumab étaient des cas de fatigue (30,0 %), des nausées (23,6 %), des diarrhées (18,5 %), une constipation (18,1 %), une diminution de l’appétit (17,6 %), des réactions liées à la perfusion (15,9 %), des vomissements (15,6 %) et une perte de poids (14,5 %).
Les effets indésirables de grade ≥ 3 les plus fréquents étaient une anémie (5,6 %), une hypertension (3,9 %), une hyponatrémie (3,6 %), une dyspnée (3,5 %) et des douleurs abdominales (2,6 %). Les effets indésirables graves étaient des effets indésirables à médiation immunitaire et des réactions liées à la perfusion (voir rubrique 4.4).
Tableau récapitulatif des effets indésirables
La sécurité de l’avélumab en monothérapie a été évaluée chez 2 082 patients atteints de tumeurs solides, dont le CCM métastatique ou le CU localement avancé ou métastatique, ayant reçu 10 mg/kg d’avélumab toutes les 2 semaines dans le cadre des études cliniques ou de l’utilisation post-commercialisation de l’avélumab (voir Tableau 2).
Ces réactions sont présentées par classe de système d’organe et par fréquence. Les fréquences sont définies comme suit : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1 000, < 1/100) ; rare (≥ 1/10 000, < 1/1 000) ; très rare (< 1/10 000) ; fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Au sein de chaque catégorie de fréquence, les effets indésirables sont présentés par ordre de gravité décroissante.
Tableau 2 : Effets indésirables survenus chez les patients traités par avélumab en monothérapie
Fréquence | Effets indésirables |
Affections hématologiques et du système lymphatique | |
Très fréquent | Anémie |
Fréquent | Lymphopénie, thrombocytopénie |
Peu fréquent | Éosinophilie§ |
Fréquence indéterminée | Neutropénie* |
Affections du système immunitaire | |
Très fréquent | Réaction liée à la perfusion# |
Peu fréquent | Hypersensibilité, hypersensibilité médicamenteuse, sarcoïdose** |
Rare | Réaction anaphylactique, hypersensibilité de type I |
Affections endocriniennes | |
Fréquent | Hypothyroïdie*, hyperthyroïdie* |
Peu fréquent | Insuffisance surrénalienne*, thyroïdite auto‑immune*, thyroïdite*, hypothyroïdie auto‑immune* |
Rare | Insuffisance corticosurrénalienne aiguë*, hypopituitarisme* |
Troubles du métabolisme et de la nutrition | |
Très fréquent | Diminution de l’appétit |
Fréquent | Hyponatrémie |
Peu fréquent | Hyperglycémie* |
Rare | Diabète*, diabète de type I* |
Affections du système nerveux | |
Fréquent | Céphalée, vertiges, neuropathie périphérique |
Peu fréquent | Myasthénie grave*†, syndrome myasthénique*† |
Rare | Syndrome de Guillain‑Barré*, syndrome de Miller‑Fisher* |
Affections oculaires | |
Rare | Uvéite* |
Affections cardiaques | |
Rare | Myocardite* |
Affections vasculaires | |
Fréquent | Hypertension |
Peu fréquent | Hypotension, bouffées vasomotrices |
Affections respiratoires, thoraciques et médiastinales | |
Très fréquent | Toux, dyspnée |
Fréquent | Pneumopathie* |
Rare | Pneumopathie interstitielle* |
Affections gastro‑intestinales | |
Très fréquent | Nausées, diarrhée, constipation, vomissements, douleur abdominale |
Fréquent | Sécheresse buccale |
Peu fréquent | Iléus, colite* |
Rare | Pancréatite*, colite auto‑immune*, entérocolite*, pancréatite auto‑immune*, entérite*, rectite* |
Fréquence indéterminée | Gastrite* |
Affections hépatobiliaires | |
Peu fréquent | Hépatite auto‑immune* |
Rare | Insuffisance hépatique aiguë*, insuffisance hépatique*, hépatite*, hépatotoxicité* |
Fréquence indéterminée | Cholangite sclérosante* |
Affections de la peau et du tissu sous‑cutané | |
Fréquent | Prurit*, éruption cutanée*, sécheresse de la peau, éruption maculo‑papuleuse* |
Peu fréquent | Eczéma, dermatite, éruption prurigineuse*, psoriasis*, érythème*, éruption érythémateuse*, éruption généralisée*, éruption maculaire*, éruption papuleuse* |
Rare | Érythème polymorphe*, purpura*, vitiligo*, prurit généralisé*, dermatite exfoliative*, pemphigoïde*, dermatite psoriasiforme*, éruption médicamenteuse*, lichen plan* |
Affections musculosquelettiques et du tissu conjonctif | |
Très fréquent | Dorsalgie, arthralgie |
Fréquent | Myalgie |
Peu fréquent | Myosite*, polyarthrite rhumatoïde* |
Rare | Arthrite*, polyarthrite*, oligoarthrite*, syndrome de Sjögren* |
Fréquence indéterminée | Pseudopolyarthrite rhizomélique* |
Affections du rein et des voies urinaires | |
Peu fréquent | Insuffisance rénale*, néphrite* |
Rare | Néphrite tubulo‑interstitielle*, cystite non infectieuse* |
Troubles généraux et anomalies au site d’administration | |
Très fréquent | Fatigue, fièvre, œdème périphérique |
Fréquent | Asthénie, frissons, syndrome pseudo‑grippal |
Rare | Syndrome de réponse inflammatoire généralisée* |
Investigations | |
Très fréquent | Perte de poids |
Fréquent | Élévation de la créatinine plasmatique, élévation de la phosphatase alcaline plasmatique, élévation de la lipase, élévation des taux de gamma‑glutamyltransférase, élévation de l’amylase |
Peu fréquent | Élévation des taux d’alanine aminotransférase (ALAT)*, élévation des taux d’aspartate aminotransférase (ASAT)*, élévation de la créatine phosphokinase plasmatique* |
Rare | Élévation des taux de transaminases*, diminution de la thyroxine libre*, augmentation de la thyréostimuline plasmatique* |
* Effet indésirable à médiation immunitaire d’après la revue médicale
** Une sarcoïdose a été observée au cours des études cliniques chez des patients ayant reçu l’avélumab en association avec une chimiothérapie à base de sel de platine
§ Réaction uniquement observée dans l’étude EMR100070‑003 (Partie B) après la date limite de recueil des données, il s’agit donc d’une estimation de la fréquence
# Y compris le syndrome de relargage des cytokines, peu fréquent
† Effets indésirables survenus chez un nombre estimé de 4 000 patients exposés à l’avélumab en monothérapie en dehors de l’analyse groupée
Carcinome à cellules rénales
Résumé du profil de sécurité
La sécurité d’emploi d’avélumab en association avec axitinib a été évaluée chez 489 patients atteints de CCR à un stade avancé ayant reçu 10 mg/kg d’avélumab toutes les 2 semaines et 5 mg d’axitinib par voie orale deux fois par jour dans deux études cliniques.
Dans cette population de patients, les effets indésirables les plus fréquents étaient la diarrhée (62,8 %), l’hypertension (49,3 %), la fatigue (42,9 %), les nausées (33,5 %), la dysphonie (32,7 %), la diminution de l’appétit (26,0 %), l’hypothyroïdie (25,2 %), la toux (23,7 %), les céphalées (21,3 %), la dyspnée (20,9 %) et les arthralgies (20,9 %).
Tableau récapitulatif des effets indésirables
Les effets indésirables rapportés chez les 489 patients atteints de CCR à un stade avancé et traités par avélumab en association avec axitinib au cours de deux études cliniques et dans le cadre de l’utilisation post-commercialisation de l’avélumab sont présentés dans le Tableau 3.
Ces réactions sont présentées par classe de système d’organe et par fréquence. Les fréquences sont définies comme suit : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1 000, < 1/100) ; rare (≥ 1/10 000, < 1/1 000) ; très rare (< 1/10 000) ; fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Au sein de chaque catégorie de fréquence, les effets indésirables sont présentés par ordre de gravité décroissante.
Tableau 3 : Effets indésirables survenus chez les patients traités par avélumab en association avec axitinib
Fréquence | Effets indésirables |
Infections et infestations | |
Peu fréquent | Eruption pustuleuse* |
Affections hématologiques et du système lymphatique | |
Fréquent | Anémie, thrombocytopénie |
Peu fréquent | Lymphopénie, éosinophilie |
Fréquence indéterminée | Neutropénie* |
Affections du système immunitaire | |
Très fréquent | Réaction liée à la perfusion# |
Fréquent | Hypersensibilité |
Affections endocriniennes | |
Très fréquent | Hypothyroïdie* |
Fréquent | Hyperthyroïdie*, insuffisance surrénalienne*, thyroïdite* |
Peu fréquent | Thyroïdite auto‑immune*, hypophysite* |
Troubles du métabolisme et de la nutrition | |
Très fréquent | Diminution de l’appétit |
Fréquent | Hyperglycémie* |
Peu fréquent | Diabète*, diabète de type I* |
Affections du système nerveux | |
Très fréquent | Céphalée, vertiges |
Fréquent | Neuropathie périphérique |
Peu fréquent | Myasthénie grave*, syndrome myasthénique* |
Affections cardiaques | |
Peu fréquent | Myocardite* |
Affections vasculaires | |
Très fréquent | Hypertension |
Fréquent | Hypotension, bouffées vasomotrices |
Affections respiratoires, thoraciques et médiastinales | |
Très fréquent | Dysphonie, toux, dyspnée |
Fréquent | Pneumopathie* |
Affections gastro‑intestinales | |
Très fréquent | Diarrhée, nausées, constipation, vomissements, douleur abdominale |
Fréquent | Sécheresse buccale, colite* |
Peu fréquent | Colite auto‑immune*, pancréatite auto‑immune*, entérocolite*, iléus, pancréatite nécrosante* |
Fréquence indéterminée | Gastrite* |
Affections hépatobiliaires | |
Fréquent | Fonction hépatique anormale* |
Peu fréquent | Hépatite*, hépatotoxicité*, hépatite à médiation immunitaire*, trouble hépatique* |
Fréquence indéterminée | Cholangite sclérosante* |
Affections de la peau et du tissu sous‑cutané | |
Très fréquent | Éruption cutanée*, prurit* |
Fréquent | Éruption prurigineuse*, éruption maculo‑papuleuse*, prurit généralisé*, dermatite acnéiforme, érythème*, éruption maculaire*, éruption papuleuse*, éruption érythémateuse*, dermatite*, eczéma, éruption généralisée* |
Peu fréquent | Éruption d’origine médicamenteuse*, érythème polymorphe*, psoriasis* |
Affections musculosquelettiques et du tissu conjonctif | |
Très fréquent | Arthralgie, dorsalgie, myalgie |
Peu fréquent | Arthrite* |
Fréquence indéterminée | Pseudopolyarthrite rhizomélique*, syndrome de Sjögren* |
Affections du rein et des voies urinaires | |
Fréquent | Insuffisance rénale aiguë* |
Troubles généraux et anomalies au site d’administration | |
Très fréquent | Fatigue, frissons, asthénie, fièvre |
Fréquent | Œdème périphérique, syndrome pseudo‑grippal |
Investigations | |
Très fréquent | Perte de poids, élévation des taux d’alanine aminotransférase (ALAT)*, élévation des taux d’aspartate aminotransférase (ASAT)* |
Fréquent | Élévation de la créatinine plasmatique, élévation de l’amylase, élévation de la lipase, élévation de la gamma‑glutamyltransférase, élévation de la phosphatase alcaline plasmatique, élévation de la créatine phosphokinase plasmatique*, diminution de la thyréostimuline (TSH) plasmatique*, élévation des taux de transaminases* |
Peu fréquent | Augmentation des paramètres biologiques du bilan hépatique* |
* Effet indésirable à médiation immunitaire d’après la revue médicale
# Y compris le syndrome de relargage des cytokines, de fréquence indéterminée
Description de certains effets indésirables particuliers
Les données relatives aux effets indésirables à médiation immunitaire pour avélumab en monothérapie reposent sur 2 082 patients, dont 1 650 patients atteints de tumeurs solides dans l’étude de phase I EMR100070‑001, 88 patients dans l’étude EMR100070‑003 sur le CCM et 344 patients dans l’étude B9991001 sur le CU et, pour l’avélumab en association avec axitinib, sur les 489 patients des études B9991002 et B9991003 sur le CCR (voir rubrique 5.1).
Les recommandations pour la prise en charge de ces effets indésirables sont décrites dans la rubrique 4.4.
Pneumopathie à médiation immunitaire
Chez les patients traités par avélumab en monothérapie, des pneumopathies à médiation immunitaire ont été observées chez 1,3 % (28/2 082) des patients. L’issue a été fatale pour 1 de ces patients (moins de 0,1 %). La pneumopathie à médiation immunitaire était de grade 4 chez 1 patient (moins de 0,1 %) et de grade 3 chez 6 patients (0,3 %).
Le délai médian d’apparition de la pneumopathie à médiation immunitaire était de 2,5 mois (intervalle : 3 jours à 13,8 mois). La durée médiane de la réaction était de 8,1 semaines (intervalle : 4 jours à plus de 4,9 mois).
L’administration d’avélumab a été interrompue chez 0,4 % (9/2 082) des patients en raison d’une pneumopathie à médiation immunitaire. Les 28 patients ayant présenté une pneumopathie à médiation immunitaire ont tous été traités par corticothérapie et 21 (75 %) des 28 patients ont reçu une corticothérapie à forte dose pendant une durée médiane de 9 jours (intervalle : 1 jour à 2,3 mois). La pneumopathie à médiation immunitaire était résolue chez 18 (64,3 %) des 28 patients à la date limite de recueil des données.
Chez les patients traités par avélumab en association avec axitinib, des pneumopathies à médiation immunitaire ont été observées chez 0,6 % (3/489) des patients. Aucun d’entre eux n’a présenté une pneumopathie à médiation immunitaire de grade ≥ 3.
Le délai médian d’apparition de la pneumopathie à médiation immunitaire était de 3,7 mois (intervalle : 2,7 mois à 8,6 mois). La durée médiane de la réaction était de 2,6 mois (intervalle : 3,3 semaines à plus de 7,9 mois).
L’administration d’avélumab n’a été interrompue chez aucun patient en raison d’une pneumopathie à médiation immunitaire. Les 3 patients ayant présenté une pneumopathie à médiation immunitaire ont été traités par une corticothérapie à forte dose pendant une durée médiane de 3,3 mois (intervalle : 3 semaines à 22,3 mois). La pneumopathie à médiation immunitaire était résolue chez 2 (66,7 %) des 3 patients à la date limite de recueil des données.
Hépatite à médiation immunitaire
Chez les patients traités par avélumab en monothérapie, des hépatites à médiation immunitaire ont été observées chez 1,0 % (21/2 082) des patients. L’issue a été fatale pour 2 de ces patients (0,1 %), et l’hépatite à médiation immunitaire était de grade 3 chez 16 patients (0,8 %).
Le délai médian d’apparition de l’hépatite à médiation immunitaire était de 3,3 mois (intervalle : 9 jours à 14,8 mois). La durée médiane de la réaction était de 2,5 mois (intervalle : 1 jour à plus de 7,4 mois).
L’administration d’avélumab a été interrompue chez 0,6 % (13/2 082) des patients en raison d’une hépatite à médiation immunitaire. Les 21 patients ayant présenté une hépatite à médiation immunitaire ont tous été traités par corticothérapie et 20 (95,2 %) des 21 patients ont reçu une corticothérapie à forte dose pendant une durée médiane de 17 jours (intervalle : 1 jour à 4,1 mois). L’hépatite à médiation immunitaire était résolue chez 12 (57,1 %) des 21 patients à la date limite de recueil des données.
Chez les patients traités par avélumab en association avec axitinib, des hépatites à médiation immunitaire ont été observées chez 6,3 % (31/489) des patients. L’hépatite à médiation immunitaire était de grade 3 chez 18 de ces patients (3,7 %) et de grade 4 chez 3 patients (0,6 %).
Le délai médian d’apparition de l’hépatite à médiation immunitaire était de 2,3 mois (intervalle : 2,1 semaines à 14,5 mois). La durée médiane de la réaction était de 2,1 semaines (intervalle : 2 jours à 8,9 mois).
L’administration d’avélumab a été interrompue chez 4,7 % (23/489) des patients en raison d’une hépatite à médiation immunitaire. Les 31 patients ayant présenté une hépatite à médiation immunitaire ont tous été traités : 30 (96,8 %) patients ont reçu une corticothérapie et 1 patient a reçu un immunosuppresseur non stéroïdien. Vingt‑huit (90,3 %) des 31 patients ont suivi une corticothérapie à forte dose pendant une durée médiane de 2,4 semaines (intervalle : 1 jour à 10,2 mois). L’hépatite à médiation immunitaire était résolue chez 27 (87,1 %) des 31 patients à la date limite de recueil des données.
Colite à médiation immunitaire
Chez les patients traités par avélumab en monothérapie, des colites à médiation immunitaire ont été observées chez 1,5 % (31/2 082) des patients. Chez 10 de ces patients (0,5 %), la colite à médiation immunitaire a été de grade 3.
Le délai médian d’apparition de la colite à médiation immunitaire était de 2,0 mois (intervalle : 2 jours à 11,5 mois). La durée médiane de la réaction était de 5,9 semaines (intervalle : 1 jour à plus de 14 mois).
L’administration d’avélumab a été interrompue chez 0,5 % (11/2 082) des patients en raison d’une colite à médiation immunitaire. Les 31 patients ayant présenté une colite à médiation immunitaire ont tous été traités par corticothérapie et 19 (61,3 %) des 31 patients ont reçu une corticothérapie à forte dose pendant une durée médiane de 19 jours (intervalle : 1 jour à 2,3 mois). La colite à médiation immunitaire était résolue chez 22 (71 %) des 31 patients à la date limite de recueil des données.
Chez les patients traités par avélumab en association avec axitinib, des colites à médiation immunitaire ont été observées chez 2,7 % (13/489) des patients. La colite à médiation immunitaire a été de grade 3 chez 9 (1,8 %) de ces patients.
Le délai médian d’apparition de la colite à médiation immunitaire était de 5,1 mois (intervalle : 2,3 semaines à 14 mois). La durée médiane de la réaction était de 1,6 semaine (intervalle : 1 jour à plus de 9 mois).
L’administration d’avélumab a été interrompue chez 0,4 % (2/489) des patients en raison d’une colite à médiation immunitaire. Les 13 patients ayant présenté une colite à médiation immunitaire ont tous été traités par corticothérapie et 12 (92,3 %) des 13 patients ont reçu une corticothérapie à forte dose pendant une durée médiane de 2,3 semaines (intervalle : 5 jours à 4,6 mois). La colite à médiation immunitaire était résolue chez 10 (76,9 %) des 13 patients à la date limite de recueil des données.
Pancréatite à médiation immunitaire
Chez les patients traités par avélumab en monothérapie, des pancréatites à médiation immunitaire ont été observées chez moins de 1 % (1/4 000) des patients dans les études cliniques avec différents types de tumeurs et chez 0,6 % (3/489) des patients ayant reçu avélumab en association avec axitinib, l’issue ayant été fatale pour 2 (0,4 %) de ces 3 patients.
Myocardite à médiation immunitaire
Chez les patients traités par avélumab en monothérapie, des myocardites à médiation immunitaire ont été observées chez moins de 1 % (5/4 000) des patients dans les études cliniques avec différents types de tumeurs et chez 0,6 % (3/489) des patients ayant reçu avélumab en association avec axitinib, l’issue ayant été fatale chez 2 (0,4 %) de ces 3 patients.
Endocrinopathies à médiation immunitaire
Troubles thyroïdiens
Chez les patients traités par avélumab en monothérapie, 6,7 % (140/2 082) des patients ont présenté des troubles thyroïdiens à médiation immunitaire, incluant 127 patients (6,1 %) avec une hypothyroïdie, 23 patients (1,1 %) avec une hyperthyroïdie et 7 patients (0,3 %) avec une thyroïdite. Les troubles thyroïdiens à médiation immunitaire ont été de grade 3 chez 4 patients (0,2 %).
Le délai médian d’apparition des troubles thyroïdiens était de 2,8 mois (intervalle : 2 semaines à 12,8 mois). La durée médiane de la réaction n’a pu être évaluée (intervalle : 3 jours à plus de 27,6 mois).
L’administration d’avélumab a été interrompue chez 0,2 % (4/2 082) des patients en raison de troubles thyroïdiens à médiation immunitaire. Les troubles thyroïdiens étaient résolus chez 14 (10 %) des 140 patients à la date limite de recueil des données.
Chez les patients traités par avélumab en association avec axitinib, des troubles thyroïdiens à médiation immunitaire ont été observés chez 24,7 % (121/489) des patients, incluant 111 patients (22,7 %) avec une ’hypothyroïdie, 17 patients (3,5 %) avec une hyperthyroïdie et 7 patients (1,4 %) avec une thyroïdite. Les troubles thyroïdiens à médiation immunitaire ont été de grade 3 chez 2 (0,4%) de ces patients.
Le délai médian d’apparition des troubles thyroïdiens était de 2,8 mois (intervalle : 3,6 semaines à 19,3 mois). La durée médiane de la réaction n’a pas pu être évaluée (intervalle : 8 jours à plus de 23,9 mois).
L’administration d’avélumab a été interrompue chez 0,2 % (1/489) des patients en raison de troubles thyroïdiens à médiation immunitaire. Les troubles thyroïdiens étaient résolus chez 15 (12,4 %) des 121 patients à la date limite de recueil des données.
Insuffisance surrénalienne
Chez les patients traités par avélumab en monothérapie, une insuffisance surrénalienne à médiation immunitaire a été observée chez 0,5 % (11/2 082) des patients. L’insuffisance surrénalienne à médiation immunitaire a été de grade 3 chez 1 patient (moins de 0,1 %).
Le délai médian d’apparition de l’insuffisance surrénalienne à médiation immunitaire était de 3,3 mois (intervalle : 1 jour à 7,6 mois). La durée médiane de la réaction n’a pu être évaluée (intervalle : 2 jours à plus de 10,4 mois).
L’administration d’avélumab a été interrompue chez 0,1 % (2/2 082) des patients en raison d’une insuffisance surrénalienne à médiation immunitaire. Les 11 patients ayant présenté une insuffisance surrénalienne à médiation immunitaire ont tous été traités par corticothérapie, et 5 (45,5 %) des 11 patients ont reçu de fortes doses de corticoïdes à action systémique (≥ 40 mg de prednisone ou équivalent) sur une durée médiane de 2 jours (intervalle : 1 jour à 24 jours). L’insuffisance surrénalienne était résolue chez 3 (27,3 %) des patients à la date limite de recueil des données.
Chez les patients traités par avélumab en association avec axitinib, une insuffisance surrénalienne à médiation immunitaire a été observée chez 1,8 % (9/489) des patients. L’insuffisance surrénalienne à médiation immunitaire a été de grade 3 chez 2 (0,4 %) de ces patients.
Le délai médian d’apparition de l’insuffisance surrénalienne à médiation immunitaire était de 5,5 mois (intervalle : 3,6 semaines à 8,7 mois). La durée médiane de la réaction était de 2,8 mois (intervalle : 3 jours à 15,5 mois).
L’administration d’avélumab n’a été interrompue chez aucun patient en raison d’une insuffisance surrénalienne à médiation immunitaire. Huit patients (88,9 %) ayant présenté une insuffisance surrénalienne à médiation immunitaire ont été traités par corticothérapie et 2 (25 %) des 8 patients ont reçu de fortes doses de corticoïdes (≥ 40 mg de prednisone ou équivalent) pendant une durée médiane de 8 jours (intervalle : 5 jours à 11 jours). L’insuffisance surrénalienne était résolue chez 4 (44,4 %) des 9 patients à la date limite de recueil des données.
Diabète de type 1
Chez les patients traités par avélumab en monothérapie, des cas de diabète de type 1 sans autre étiologie connue ont été observés chez 0,2 % (5/2 082) des patients. Les 5 patients ont tous présenté un diabète de type 1 de grade 3.
Le délai médian d’apparition du diabète de type 1 était de 3,3 mois (intervalle : 1 jour à 18,7 mois). La durée médiane de la réaction n’a pu être évaluée (intervalle : 14 jours à plus de 4,8 mois).
L’administration d’avélumab a été interrompue chez 0,1 % (2/2 082) des patients en raison d’un diabète de type 1. Le diabète de type 1 était résolu chez 2 (40 %) des patients à la date limite de recueil des données.
Chez les patients traités par avélumab en association avec axitinib, un diabète de type 1 sans autre étiologie connue a été observé chez 1,0 % (5/489) des patients. Le diabète de type 1 était de grade 3 chez 1 (0,2 %) de ces patients.
Le délai médian d’apparition du diabète de type 1 était de 1,9 mois (intervalle : 1,1 mois à 7,3 mois).
L’administration d’avélumab a été interrompue chez 0,2 % (1/489) des patients en raison d’un diabète de type 1. Les 5 patients ayant présenté un diabète de type 1 ont tous été traités par insuline. Le diabète de type 1 n’était résolu chez aucun des patients au moment de la date limite de recueil des données.
Néphrite et dysfonction rénale à médiation immunitaire
Chez les patients traités par avélumab en monothérapie, des cas de néphrite à médiation immunitaire ont été observés chez 0,3 % (7/2 082) des patients. La néphrite à médiation immunitaire a été de grade 3 chez 1 (moins de 0,1 %) patient.
Le délai médian d’apparition de la néphrite à médiation immunitaire était de 2,4 mois (intervalle :7,1 semaines à 21,9 mois). La durée médiane de la réaction était de 6,1 mois (intervalle : 9 jours à 6,1 mois).
L’administration d’avélumab a été interrompue chez 0,2 % (4/2 2082) des patients en raison d’une néphrite à médiation immunitaire. Les 7 patients ayant présenté une néphrite à médiation immunitaire ont tous été traités par corticothérapie. 6 (85,7 %) des 7 patients ayant présenté une néphrite à médiation immunitaire ont reçu de fortes doses de corticoïdes sur une durée médiane de 2,5 semaines (intervalle : 6 jours à 2,8 mois). La néphrite à médiation immunitaire était résolue chez 4 (57,1 %) patients à la date limite de recueil des données.
Chez les patients traités par avélumab en association avec axitinib, une néphrite à médiation immunitaire a été observée chez 0,4 % (2/489) des patients. La néphrite à médiation immunitaire était de grade 3 chez 2 (0,4 %) de ces patients.
Le délai médian d’apparition de la néphrite à médiation immunitaire était de 1,2 mois (intervalle : 2,9 semaines à 1,8 mois). La durée médiane de la réaction était de 1,3 semaine (intervalle : plus de 4 jours à 1,3 semaine).
L’administration d’avélumab n’a été interrompue chez aucun patient en raison d’une néphrite à médiation immunitaire. Les 2 patients ayant présenté une néphrite à médiation immunitaire ont tous les deux été traités par de fortes doses de corticoïdes pendant une durée médiane de 1,1 semaine (intervalle : 3 jours à 1,9 semaine). La néphrite à médiation immunitaire était résolue chez 1 (50 %) des 2 patients au moment de la date limite de recueil des données.
Hépatotoxicité (en association avec axitinib)
Chez les patients traités par avélumab en association avec axitinib, une augmentation des taux d’ALAT et d’ASAT de grade 3 et de grade 4 a été rapportée chez, respectivement, 9 % et 7 % des patients.
Chez les patients ayant présenté un taux d’ALAT ≥ 3 fois la LNS (grades 2‑4, n = 82), le taux d’ALAT a régressé à un grade 0‑1 dans 92 % des cas.
Parmi les 73 patients traités de nouveau par avélumab (59 %) ou axitinib (85 %) en monothérapie, ou les deux (55 %), 66 % n’ont pas montré de nouvelle augmentation du taux d’ALAT ≥ 3 fois la LNS.
Effets de la classe des inhibiteurs de point de contrôle immunitaire
Des cas avec l’effet indésirable suivant ont été rapportés au cours du traitement par d’autres inhibiteurs de point de contrôle immunitaire, qui peuvent également survenir au cours du traitement par avélumab : insuffisance pancréatique exocrine, maladie coeliaque.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via
Belgique :
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg :
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Merck Europe B.V.
Gustav Mahlerplein 102
1082 MA Amsterdam
Pays‑Bas
8. NUMERO D’AUTORISATION DE MISE SUR LE MARCHE
EU/1/17/1214/001
10. DATE DE MISE A JOUR DU TEXTE
11/2025
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments https://www.ema.europa.eu.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 3705043 | BAVENCIO 20MG/ML SOL PERF FL INJ IV 1 X 10ML | L01FF04 | - | € 777,95 | Oui | - | - |