1. DÉNOMINATION DU MÉDICAMENT
Entresto 24 mg/26 mg, comprimés pelliculés
Entresto 49 mg/51 mg, comprimés pelliculés
Entresto 97 mg/103 mg, comprimés pelliculés
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Entresto 24 mg/26 mg, comprimés pelliculés
Chaque comprimé pelliculé contient 24,3 mg de sacubitril et 25,7 mg de valsartan (sous forme de complexe sodique sacubitril valsartan).
Entresto 49 mg/51 mg, comprimés pelliculés
Chaque comprimé pelliculé contient 48,6 mg de sacubitril et 51,4 mg de valsartan (sous forme de complexe sodique sacubitril valsartan).
Entresto 97 mg/103 mg, comprimés pelliculés
Chaque comprimé pelliculé contient 97,2 mg de sacubitril et 102,8 mg de valsartan (sous forme de complexe sodique sacubitril valsartan).
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Comprimé pelliculé (comprimé).
Entresto 24 mg/26 mg, comprimés pelliculés
Comprimé pelliculé violet blanc, ovale, biconvexe, à bords biseautés, non sécable, portant l’inscription « NVR » gravée sur une face et « LZ » sur l’autre face. Dimensions approximatives du comprimé de 13,1 mm x 5,2 mm.
Entresto 49 mg/51 mg, comprimés pelliculés
Comprimé pelliculé jaune pâle, ovale, biconvexe, à bords biseautés, non sécable, portant l’inscription « NVR » gravée sur une face et « L1 » sur l’autre face. Dimensions approximatives du comprimé de 13,1 mm x 5,2 mm.
Entresto 97 mg/103 mg, comprimés pelliculés
Comprimé pelliculé rose clair, ovale, biconvexe, à bords biseautés, non sécable, portant l’inscription « NVR » gravée sur une face et « L11 » sur l’autre face. Dimensions approximatives du comprimé de 15,1 mm x 6,0 mm.
4. INFORMATIONS CLINIQUES
4.1 Indications thérapeutiques
Insuffisance cardiaque chez l’adulte
Entresto est indiqué chez les patients adultes dans le traitement de l’insuffisance cardiaque chronique symptomatique à fraction d’éjection réduite (voir rubrique 5.1).
Insuffisance cardiaque pédiatrique
Entresto est indiqué chez les enfants et adolescents âgés d’un an ou plus dans le traitement de l’insuffisance cardiaque chronique symptomatique avec dysfonction systolique ventriculaire gauche (voir rubrique 5.1).
4.2 Posologie et mode d’administration
Posologie
Observations générales
Entresto ne doit pas être administré de façon concomitante avec un inhibiteur de l’enzyme de conversion (IEC) ou un antagoniste du récepteur de l’angiotensine II (ARAII). Compte tenu du risque potentiel d’angiœdème lors de l’administration concomitante d’un IEC, il doit être initié au moins 36 heures après l’arrêt du traitement par IEC (voir rubriques 4.3, 4.4 et 4.5).
Le valsartan contenu dans Entresto a une bioéquivalence supérieure à celle du valsartan contenu dans d’autres formulations de comprimés commercialisés (voir rubrique 5.2).
En cas d’oubli d’une dose d’Entresto, le patient doit prendre la dose suivante à l’heure habituelle.
Insuffisance cardiaque chez l’adulte
La dose initiale recommandée d’Entresto est d’un comprimé de 49 mg/51 mg deux fois par jour, à l’exception des situations décrites ci-dessous. La dose d’Entresto doit être doublée toutes les 2 à 4 semaines jusqu’à la dose cible de 97 mg/103 mg deux fois par jour, en fonction de la tolérance du patient (voir rubrique 5.1).
En cas de problèmes de tolérance (pression artérielle systolique [PAS] ≤95 mmHg, hypotension symptomatique, hyperkaliémie, altération de la fonction rénale), une adaptation posologique des traitements concomitants, une diminution temporaire de la dose ou un arrêt d’Entresto est recommandé (voir rubrique 4.4).
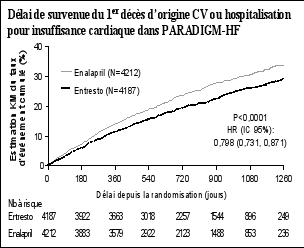
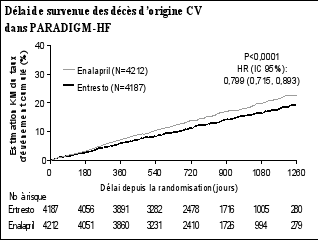
Dans l’étude PARADIGM-HF, Entresto était administré en remplacement d’un IEC ou d’autres ARAII et en association avec d’autres thérapies de l’insuffisance cardiaque (voir rubrique 5.1). Compte-tenu de l’expérience limitée chez les patients n’étant pas actuellement traités par un IEC ou un ARAII, ou prenant ces médicaments à faible dose, une dose initiale de 24 mg/26 mg deux fois par jour d’Entresto et une lente augmentation de la dose (doublement de la posologie toutes les 3 à 4 semaines) sont recommandées chez ces patients (voir « TITRATION » en rubrique 5.1).
Le traitement ne doit pas être initié chez les patients ayant une kaliémie >5,4 mmol/l ou une PAS 100 mmHg (voir rubrique 4.4). Une dose initiale de 24 mg/26 mg deux fois par jour doit être envisagée chez les patients ayant une PAS comprise entre 100 et 110 mmHg.
Insuffisance cardiaque pédiatrique
Le tableau 1 présente la dose recommandée pour les patients pédiatriques. La dose recommandée doit être prise oralement deux fois par jour. La dose d’Entresto doit être augmentée toutes les 2 à 4 semaines jusqu’à la dose cible, en fonction de la tolérance du patient.
Entresto sous forme de comprimés pelliculés n’est pas adapté aux enfants de moins de 40 kg. Entresto sous forme de granulés est disponible pour ces patients.
Tableau 1 Recommandations de titration de dose
Poids du patient | A administrer deux fois par jour | |||
Moitié de la dose initiale* | Dose initiale | Dose intermédiaire | Dose cible | |
Enfants de moins de 40 kg | 0,8 mg/kg# | 1,6 mg/kg# | 2,3 mg/kg# | 3,1 mg/kg# |
Enfants de 40 kg à moins de 50 kg | 0,8 mg/kg# | 24 mg/26 mg | 49 mg/51 mg | 72 mg/78 mg |
Enfants de 50 kg et plus | 24 mg/26 mg | 49 mg/51 mg | 72 mg/78 mg | 97 mg/103 mg |
* La moitié de la dose initiale est recommandée chez les patients non traités par un IEC ou un ARA II ou ayant pris des faibles doses de ces derniers, chez les patients ayant une insuffisance rénale (débit de filtration glomérulaire estimé (DFGe) <60 mL/min/1,73 m²) et chez les patients ayant une insuffisance hépatique modérée (voir « Populations particulières »).
#0,8 mg/kg, 1,6 mg/kg, 2,3 mg/kg et 3,1 mg/kg correspondent à la quantité combinée de sacubitril et de valsartan et doivent être administrés sous forme de granulés.
Chez les patients actuellement non traités par un IEC ou un ARA II ou prenant des faibles doses de ces derniers, la moitié de la dose initiale est recommandée. Pour les enfants de 40 kg à moins de 50 kg, une dose initiale de 0,8 mg/kg deux fois par jour (sous forme de granulés) est recommandée. Après initiation, la dose doit être augmentée jusqu’au palier suivant en suivant les recommandations de titration de dose du Tableau 1 et être ajustée toutes les 3 à 4 semaines.
Par exemple, un patient pédiatrique pesant 25 kg non traité précédemment par un IEC doit débuter avec la moitié de la dose initiale standard, correspondant à 20 mg (25 kg x 0,8 mg/kg) deux fois par jour, sous forme de granulés. Après avoir arrondi au nombre le plus proche de gélules entières, cela correspond à 2 gélules de sacubitril/valsartan de 6 mg/6 mg deux fois par jour.
Le traitement ne doit pas être instauré chez les patients ayant une kaliémie >5,3 mmol/l ou une PAS <5ème percentile de l’âge du patient. Si les patients présentent des problèmes de tolérance (PAS <5ème percentile de l’âge du patient, hypotension symptomatique, hyperkaliémie, dysfonctionnement rénal), un ajustement des médicaments concomitants, une diminution temporaire de la dose ou l’arrêt d’Entresto est recommandé (voir rubrique 4.4).
Populations particulières
Sujets âgés
La dose doit être adaptée à l’état de la fonction rénale du patient âgé.
Insuffisance rénale
Aucune adaptation posologique n’est nécessaire chez les patients atteints d’insuffisance rénale légère (DFGe de 60‑90 ml/min/1,73 m2).
La moitié de la dose initiale doit être envisagée chez les patients atteints d’insuffisance rénale modérée (DFGe de 30‑60 ml/min/1,73 m2). L’expérience clinique étant très limitée chez les patients atteints d’insuffisance rénale sévère (DFGe < 30 ml/min/1,73 m2) (voir rubrique 5.1), Entresto doit être administré avec précaution et la moitié de la dose initiale est recommandée. Chez les enfants de 40 kg à moins de 50 kg, une dose initiale de 0,8 mg/kg deux fois par jour (sous forme de granulés) est recommandée. Après initiation, la dose doit être augmentée en suivant les recommandations de titration toutes les 2 à 4 semaines.
Il n’y a pas d’expérience chez les patients atteints d’insuffisance rénale terminale et l’administration d’Entresto n’est pas recommandée.
Insuffisance hépatique
Aucune adaptation posologique n’est nécessaire chez les patients présentant une insuffisance hépatique légère (classe A de Child-Pugh).
En raison de l’expérience limitée chez les patients atteints d’insuffisance hépatique modérée (classe B de Child-Pugh) ou ayant des valeurs des aspartate aminotransférase (ASAT)/alanine aminotransférase (ALAT) deux fois supérieures à la limite normale supérieure, Entresto doit être utilisé avec précaution chez ces patients et la moitié de la dose initiale est recommandée (voir rubriques 4.4 et 5.2). Chez les enfants de 40 kg à moins de 50 kg, une dose initiale de 0,8 mg/kg deux fois par jour (sous forme de granulés) est recommandée. Après initiation, la dose doit être augmentée en suivant les recommandations de titration toutes les 2 à 4 semaines.
Entresto est contre-indiqué chez les patients atteints d’insuffisance hépatique sévère, d’une cirrhose biliaire ou d’une cholestase (classe C de Child-Pugh) (voir rubrique 4.3).
Population pédiatrique
La sécurité et l’efficacité d’Entresto chez les enfants de moins de 1 an n’ont pas encore été établies. Les données actuellement disponibles sont décrites à la rubrique 5.1 mais aucune recommandation sur la posologie ne peut être donnée.
Mode d’administration
Voie orale.
Entresto peut être administré pendant ou en dehors des repas (voir rubrique 5.2). Les comprimés doivent être avalés avec un verre d’eau. Le fractionnement ou l’écrasement des comprimés n’est pas recommandé.
4.3 Contre-indications
- Hypersensibilité aux substances actives, ou à l’un des excipients mentionnés à la rubrique 6.1.
- Utilisation concomitante d’IEC (voir rubriques 4.4 et 4.5). Entresto ne doit être administré que 36 heures après l’arrêt de l’IEC.
- Antécédent d’angiœdème lié à un traitement antérieur par IEC ou ARA II (voir rubrique 4.4).
- Angiœdème héréditaire ou idiopathique (voir rubrique 4.4)
- Utilisation concomitante de médicaments contenant de l’aliskiren chez les patients atteints de diabète ou d’insuffisance rénale (DFGe < 60 ml/min/1,73 m2) (voir rubriques 4.4 et 4.5).
- Insuffisance hépatique sévère, cirrhose biliaire ou cholestase (voir rubrique 4.2).
- Deuxième et troisième trimestres de la grossesse (voir rubrique 4.6).
4.8 Effets indésirables
Résumé du profil de tolérance
Les effets indésirables les plus fréquemment rapportés chez les adultes pendant le traitement par sacubitril/valsartan ont été l’hypotension (17,6 %), l’hyperkaliémie (11,6 %) et une altération de la fonction rénale (10,1 %) (voir rubrique 4.4). Des angiœdèmes ont été rapportés chez les patients traités avec sacubitril/valsartan (0,5 %) (voir description des effets indésirables spécifiques).
Tableau des effets indésirables
Les effets indésirables sont classés selon le système de classification par organe et au sein de chaque classe par ordre décroissant de fréquence, selon la convention suivante : très fréquent (≥ 1/10), fréquent (≥ 1/100, <1/10), peu fréquent (≥ 1/1 000, < 1/100), rare (≥ 1/10 000, < 1/1 000), très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Dans chaque catégorie de fréquence, les effets indésirables sont classés par ordre décroissant de gravité.
Tableau 2 Liste des effets indésirables
Classe de systèmes d’organes | Terme préférentiel | Fréquence |
Affections hématologiques et du système lymphatique | Anémie | Fréquent |
Affections du système immunitaire | Hypersensibilité | Peu fréquent |
Troubles du métabolisme et de la nutrition | Hyperkaliémie* | Très fréquent |
Hypokaliémie | Fréquent | |
Hypoglycémie | Fréquent | |
Hyponatrémie | Peu fréquent | |
Troubles psychiatriques | Hallucinations** | Rare |
Troubles du sommeil | Rare | |
Paranoïa | Très rare | |
Affections du système nerveux | Sensation vertigineuse | Fréquent |
Céphalée | Fréquent | |
Syncope | Fréquent | |
Sensation vertigineuse posturale | Peu fréquent | |
Myoclonie | Fréquence indéterminée | |
Affections de l’oreille et du labyrinthe | Vertige | Fréquent |
Affections vasculaires | Hypotension* | Très fréquent |
Hypotension orthostatique | Fréquent | |
Affections respiratoires, thoraciques et médiastinales | Toux | Fréquent |
Affections gastro-intestinales | Diarrhée | Fréquent |
Nausées | Fréquent | |
Gastrite | Fréquent | |
Angiœdème intestinal | Très rare | |
Affections de la peau et du tissu sous-cutané | Prurit | Peu fréquent |
Rash | Peu fréquent | |
Angiœdème* | Peu fréquent | |
Affections du rein et des voies urinaires | Altération de la fonction rénale* | Très fréquent |
Insuffisance rénale (insuffisance rénale, insuffisance rénale aigue) | Fréquent | |
Troubles généraux et anomalies au site d’administration | Fatigue | Fréquent |
Asthénie | Fréquent |
*Voir description d’effets indésirables spécifiques.
**Y compris les hallucinations auditives et visuelles
Description d’effets indésirables spécifiques
Angiœdème
Des cas d’angiœdème ont été rapportés chez des patients traités par sacubitril/valsartan. Dans PARADIGM-HF, des angiœdèmes ont été rapportés chez 0,5 % des patients traités par sacubitril/valsartan en comparaison à 0,2 % des patients traités par énalapril. Une incidence plus élevée des angiœdèmes a été observée chez les patients noirs traités par sacubitril/valsartan (2,4 %) et énalapril (0,5 %) (voir rubrique 4.4).
Hyperkaliémie et kaliémie
Dans l’étude PARADIGM-HF, l’hyperkaliémie et la kaliémie>5.4 mmol/l ont été rapportées chez 11,6 % et 19,7 % des patients traités par sacubitril/valsartan et chez 14,0 % et 21,1 % des patients traités par énalapril, respectivement.
Pression artérielle
Dans PARADIGM-HF, l’hypotension et les diminutions de pression artérielle systolique cliniquement significatives (<90 mmHg et diminution par rapport à l’état initial de >20 mmHg) ont été rapportées chez 17,6 % et 4,76 % des patients traités par sacubitril/valsartan en comparaison à 11,9 % et 2,67 % des patients traités par énalapril, respectivement.
Insuffisance rénale
Dans PARADIGM-HF, l’altération de la fonction rénale a été rapportée chez 10,1 % des patients traités par sacubitril/valsartan et 11,5 % des patients traités par énalapril.
Population pédiatrique
Dans l’étude PANORAMA-HF, la sécurité de sacubitril/valsartan a été évaluée dans une étude randomisée, contrôlée par un comparateur actif, d’une durée de 52 semaines portant sur 375 patients pédiatriques insuffisants cardiaques (IC) âgés de 1 mois à <18 ans par rapport à l’énalapril. Les 215 patients qui ont participé à l’étude de suivi à long terme en ouvert (PANORAMA-HF OLE) ont été traités pendant une durée médiane de 2,5 ans, pouvant aller jusqu’à 4,5 ans. Le profil de sécurité observé dans les deux études était similaire à celui observé chez les patients adultes. Les données de sécurité chez les patients âgés de 1 mois à <1 an étaient limitées.
Les données de sécurité disponibles dans la population pédiatrique ayant une insuffisance hépatique modérée ou une insuffisance rénale modérée à sévère sont limitées.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via:
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy
ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet: www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHÉ
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irlande
8. NUMÉRO(S) D’AUTORISATION DE MISE SUR LE MARCHÉ
Entresto 24 mg/26 mg comprimés pelliculés
EU/1/15/1058/001
EU/1/15/1058/008‑010
EU/1/15/1058/017-018
Entresto 49 mg/51 mg comprimés pelliculés
EU/1/15/1058/002‑004
EU/1/15/1058/011‑013
EU/1/15/1058/019-020
Entresto 97 mg/103 comprimés pelliculés
EU/1/15/1058/005‑007
EU/1/15/1058/014‑016
EU/1/15/1058/021-022
10. DATE DE MISE À JOUR DU TEXTE
12.01.2026
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments https://www.ema.europa.eu.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 3277076 | ENTRESTO 24MG/ 26MG COMP PELL 28 | C09DX04 | € 69,25 | - | Oui | € 12,8 | € 8,5 |
| 3277084 | ENTRESTO 49MG/ 51MG COMP PELL 56 | C09DX04 | € 128,22 | - | Oui | € 12,8 | € 8,5 |
| 3277092 | ENTRESTO 97MG/103MG COMP PELL 56 | C09DX04 | € 128,22 | - | Oui | € 12,8 | € 8,5 |
| 4160099 | ENTRESTO 97MG/103MG COMP PELL 168 | C09DX04 | € 362,7 | - | Oui | € 15,9 | € 10,5 |
| 4160107 | ENTRESTO 49MG/ 51MG COMP PELL 168 | C09DX04 | € 362,7 | - | Oui | € 15,9 | € 10,5 |