RESUME DES CARACTERISTIQUES DU PRODUIT
1. DENOMINATION DU MEDICAMENT
Havrix Junior 720 (0,5 ml/dose), suspension injectable
Havrix Junior 720 (0,5 ml/dose), suspension injectable en seringue préremplie
Havrix 1440 (1 ml/dose), suspension injectable
Havrix 1440 (1 ml/dose), suspension injectable en seringue préremplie
Vaccin contre l’hépatite A (inactivé, adsorbé).
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Havrix Junior 720
1 dose (0,5 ml) contient :
Virus (inactivé)1,2 de l’hépatite A 720 unités ELISA
1 produit sur des cellules diploïdes humaines (MRC-5)
² adsorbé sur de l’aluminium hydroxyde, hydraté Total : 0,25 mg Al3+
Havrix 1440
1 dose (1 ml) contient :
Virus (inactivé)1,2 de l’hépatite A 1 440 unités ELISA
1 produit sur des cellules diploïdes humaines (MRC-5)
² adsorbé sur de l’aluminium hydroxyde, hydraté Total : 0,50 mg Al3+
Le vaccin peut contenir des traces de néomycine et de formaldéhyde, qui sont utilisés pendant le procédé de fabrication (voir rubrique 4.3).
Excipients à effet notoire :
Havrix Junior 720 contient 83 microgrammes de phénylalanine et 25 microgrammes de polysorbate 20 par dose (voir rubrique 4.4).
Havrix 1440 contient 166 microgrammes de phénylalanine et 50 microgrammes de polysorbate 20 par dose (voir rubrique 4.4).
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Pour le flacon :
Suspension injectable.
Pour la seringue préremplie :
Suspension injectable en seringue préremplie.
Suspension liquide trouble. Lors du stockage, un fin dépôt blanc avec un surnageant clair incolore peut être observé.
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Havrix est indiqué pour l’immunisation active contre l'infection par le virus de l’hépatite A (VHA) chez les enfants, adolescents et adultes :
- Havrix Junior 720 : chez les sujets âgés de 1 à 15 ans inclus. Il peut également être utilisé chez les adolescents jusqu'à 18 ans inclus.
- Havrix 1440 : chez les sujets âgés de 16 ans et plus.
Ce vaccin doit être utilisé conformément aux recommandations officielles.
4.2 Posologie et mode d’administration
Posologie
Primovaccination
Havrix Junior 720 (0,5 ml de suspension)
Une seule dose de Havrix Junior 720 est utilisée pour l’immunisation des enfants et des adolescents âgés de 1 à 15 ans inclus.
Il pourrait également être acceptable d’utiliser une seule dose de Havrix Junior 720 pour l’immunisation des adolescents âgés de 16 à 18 ans inclus, si nécessaire (voir rubrique 5.1).
Havrix 1440 (1,0 ml de suspension)
Une seule dose de Havrix 1440 est utilisée pour l’immunisation des adultes et des adolescents âgés de 16 ans et plus.
Pour une réponse optimale en anticorps, la dose de primovaccination doit être administrée au moins 2 semaines, et de préférence 4 semaines, avant l'exposition attendue au virus de l'hépatite A (voir rubrique 5.1).
Vaccination de rappel
Après la primovaccination avec Havrix Junior 720 ou Havrix 1440, une dose de rappel est recommandée pour assurer une protection à long terme. Cette dose de rappel doit être administrée de préférence entre 6 mois et 12 mois après la primovaccination, cependant, elle peut être administrée jusqu’à 5 ans après la primovaccination (voir rubrique 5.1).
Interchangeabilité
Havrix est interchangeable avec d’autres vaccins inactivés contre l'hépatite A.
Population âgée
Les données avec les vaccins inactivés contre l’hépatite A sont limitées chez les sujets âgés.
Population pédiatrique
La sécurité et l’efficacité de Havrix Junior 720 chez les enfants âgés de moins de 1 an n'ont pas été établies.
Les données actuellement disponibles sont décrites à la rubrique 5.1 mais aucune recommandation sur la posologie ne peut être faite.
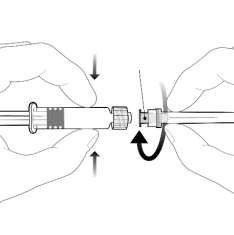
Mode d’administration
Havrix Junior 720 (0,5 ml de suspension) doit être administré par voie intramusculaire dans la région deltoïde chez les enfants et les adolescents et dans la partie antéro-latérale de la cuisse chez les jeunes enfants si le muscle deltoïde n’est pas suffisamment développé (voir rubrique 6.6).
Havrix 1440 (1,0 ml de suspension) doit être administré par voie intramusculaire dans la région deltoïde chez les adolescents et les adultes (voir rubrique 6.6).
Quel que soit le site d'administration, une pression ferme doit être appliquée sur le site d'injection (sans frotter) pendant au moins deux minutes après l'injection.
Havrix ne doit pas être administré dans la région fessière.
Havrix ne doit en aucun cas être administré par voie intravasculaire.
Havrix ne doit pas être administré par voie sous-cutanée ou intradermique (voir rubrique 4.4).
4.3 Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1 ou à la néomycine ou au formaldéhyde.
Hypersensibilité après une précédente administration de tout vaccin contre l’hépatite A.
4.8 Effets indésirables
Résumé du profil de sécurité
Les effets indésirables locaux les plus fréquents, tant chez les enfants que chez les adultes, sont la douleur et la rougeur au site d'injection.
Les effets indésirables généraux les plus fréquents sont, chez l'enfant, l'irritabilité et, chez l'adulte, la fatigue et les céphalées.
Liste tabulée des effets indésirables
Données des essais cliniques
Le profil de sécurité présenté dans le tableau ci-dessous est basé sur les données de 5 331 sujets dont 1 664 enfants (jusqu’à l’âge de 18 ans) vaccinés avec Havrix Junior 720 et 3 667 adultes (à partir de l’âge de 16 ans) vaccinés avec Havrix 1440, lors des essais cliniques (cohorte totale vaccinée). Au total, 3 193 doses de Havrix Junior 720 et 7 131 doses de Havrix 1440 ont été administrées au cours des essais cliniques. Un nombre total de 3 971 doses de Havrix 1440 ont été administrées en même temps qu'Engerix B chez 2 064 sujets adultes.
Les effets indésirables rapportés sont listés selon les fréquences suivantes :
Très fréquent (≥ 1/10)
Fréquent (≥ 1/100 à < 1/10)
Peu fréquent (≥ 1/1 000 à < 1/100)
Rare (≥ 1/10 000 à < 1/1 000)
Très rare (< 1/10 000)
Au sein de chaque groupe de fréquence, les effets indésirables sont présentés par ordre décroissant de gravité.
Classes de Systèmes d’Organes | Fréquence | Effets indésirables |
Infections et infestations | Peu fréquent | Infection des voies respiratoires supérieures (2), rhinite |
Troubles du métabolisme et de la nutrition | Fréquent | Perte d’appétit |
Affections psychiatriques | Très fréquent | Irritabilité (1) |
Affections du système nerveux | Très fréquent | Céphalées (3) |
Fréquent | Somnolence (1) | |
Peu fréquent | Vertiges (2) | |
Rare | Hypoesthésie (2), paresthésie (2) | |
Affections gastro-intestinales | Fréquent | Signes et symptômes gastro-intestinaux (2)(5), diarrhées (4), nausées |
Peu fréquent | Vomissements | |
Affections de la peau et du tissu sous-cutané | Peu fréquent | Eruption cutanée (1) |
Rare | Prurit (2) | |
Affections musculosquelettiques et du tissu conjonctif | Peu fréquent | Myalgie (2), raideur musculosquelettique (2) |
Troubles généraux et anomalies au site d’administration | Très fréquent | Douleur au site d'injection et érythème au site d'injection, fatigue (2) |
Fréquent | Malaise, fièvre (≥ 37,5°C), réaction au site d’injection (telle qu’induration au site d'injection (4) et gonflement au site d’injection) | |
Peu fréquent | Syndrome pseudo-grippal (2) | |
Rare | Frissons (2) |
(1) uniquement avec Havrix Junior 720
(2) uniquement avec Havrix 1440
(3) rapporté comme fréquente avec Havrix Junior 720
(4) rapporté comme peu fréquent avec Havrix Junior 720
(5) gastro-intestinal = incluant nausées, vomissements, diarrhées (symptômes non enregistrés séparément)
Données post-commercialisation
Les effets indésirables supplémentaires suivants ont été identifiés au cours de la surveillance post-commercialisation avec Havrix Junior 720 et Havrix 1440.
Classe de Systèmes d’Organes | Fréquence | Effets indésirables |
Affections du système immunitaire | Rare | Anaphylaxie, réactions allergiques incluant des réactions anaphylactoïdes et réaction de type maladie sérique |
Affections du système nerveux | Rare | Convulsions |
Affections vasculaires | Rare | Vasculite |
Affections de la peau et du tissu sous-cutané | Rare | Œdème angioneurotique, érythème polymorphe, urticaire |
Affections musculosquelettiques et du tissu conjonctif | Rare | Arthralgie |
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration :
Belgique | Luxembourg |
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
GlaxoSmithKline Biologicals SA
Rue de l'Institut, 89
1330 Rixensart
Belgique
8. NUMEROS D’AUTORISATION DE MISE SUR LE MARCHE
Belgique : Havrix 1440: BE167395 (seringue préremplie) - BE167386 (flacon)
Havrix Junior 720: BE180232 (seringue préremplie) - BE180223 (flacon)
Luxembourg : Havrix 1440: 2007089432
- 0206053 (1*5 seringues préremplies + 1*5 aiguilles)
- 0206067 (1*1 seringue préremplie + 1*1 aiguille)
Havrix Junior 720: 2007089433
- 0230224 (1*1 seringue préremplie + 1*1 aiguille)
10. DATE DE MISE A JOUR DU TEXTE
03/2025.
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence Fédérale des Médicaments et des Produits de Santé (AFMPS) : https://www.afmps.be/fr.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 1149939 | HAVRIX 1440 SER INJ IM 1ML | J07BC02 | € 45,66 | - | Oui | - | - |
| 1345545 | HAVRIX JUNIOR 720 SER INJ IM 0,5ML | J07BC02 | € 30,04 | - | Oui | - | - |