Résumé des caractéristiques du produit
1. DÉNOMINATION DU MÉDICAMENT
Diflucan 10 mg/ml poudre pour suspension buvable
Diflucan 40 mg/ml poudre pour suspension buvable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Diflucan 10 mg/ml poudre pour suspension buvable : 1 ml de suspension reconstituée contient 10 mg de fluconazole.
Excipients à effet notoire : 0,58 g de saccharose, 1,13 mg de sodium et 2,38 mg de benzoate de sodium par ml de suspension reconstituée.
Diflucan 40 mg/ml poudre pour suspension buvable : 1 ml de suspension reconstituée contient 40 mg de fluconazole.
Excipients à effet notoire : 0,55 g de saccharose et 2,38 mg de benzoate de sodium par ml de suspension reconstituée.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Poudre pour suspension buvable
Poudre pour suspension buvable blanche à blanc cassé, procurant une suspension blanche à blanc cassé au goût d'orange après reconstitution.
4. DONNÉES CLINIQUES
4.1 Indications thérapeutiques
Diflucan est indiqué dans les infections fongiques suivantes (voir rubrique 5.1).
Diflucan est indiqué chez les adultes dans le traitement de :
- La méningite à cryptocoques (voir rubrique 4.4).
- La coccidioïdomycose (voir rubrique 4.4).
- Les candidoses invasives.
- Les candidoses muqueuses, y compris les candidoses oropharyngées, œsophagiennes, la candidurie et les candidoses cutanéo-muqueuses chroniques.
- Les candidoses buccales atrophiques chroniques (douleurs résultant du port d'un dentier) lorsque l'hygiène dentaire ou un traitement local sont insuffisants.
- Les candidoses vaginales, aiguës ou récurrentes ; lorsqu’un traitement local n’est pas approprié.
- La balanite candidosique lorsqu’un traitement local n’est pas approprié.
- Les dermatomycoses, y compris tinea pedis, tinea corporis, tinea cruris, tinea versicolor et les infections dermiques à Candida lorsqu’un traitement systémique est indiqué.
- Tinea unguinium (onychomycose) lorsque les autres agents ne sont pas considérés comme appropriés.
Diflucan est indiqué chez les adultes dans la prophylaxie de :
- Récidive de la méningite à cryptocoques chez les patients présentant un risque élevé de rechute.
- Récidive de la candidose oropharyngée ou oesophagienne chez les patients infectés par le VIH et qui présentent un risque élevé de rechute.
- Afin de réduire l'incidence des récidives de candidose vaginale (4 épisodes ou plus par an).
- Prophylaxie des infections à Candida chez les patients avec une neutropénie prolongée (comme les patients atteints de tumeurs hématologiques malignes traités par chimiothérapie ou les patients recevant une transplantation de cellules souches hématopoïétiques (voir rubrique 5.1)).
Diflucan est indiqué chez les nouveau-nés à terme, les nourrissons, les jeunes enfants, les enfants et les adolescents, âgés de 0 à 17 ans :
Diflucan est utilisé pour le traitement des candidoses muqueuses (oropharyngées, œsophagiennes), des candidoses invasives, des méningites à cryptocoques et pour la prophylaxie des infections à Candida chez les patients immunodéprimés. Diflucan peut être utilisé comme traitement d'entretien pour prévenir les récidives de la méningite à cryptocoques chez les enfants présentant un risque élevé de rechute (voir rubrique 4.4).
Le traitement peut être instauré avant de connaître les résultats des cultures et des autres examens biologiques ; cependant, une fois que ces résultats seront disponibles, le traitement anti-infectieux devra être ajusté en conséquence.
Il convient de tenir compte des recommandations officielles concernant l’utilisation appropriée des antifongiques.
4.2 Posologie et mode d’administration
Posologie
La dose devra être basée sur la nature et la sévérité de l'infection fongique. Le traitement des infections exigeant un dosage répété devrait être poursuivi jusqu'à ce que les paramètres cliniques ou les analyses en laboratoire indiquent que l'infection fongique active a régressé. Une période inadéquate de traitement peut entraîner la récidive d'infection active.
Adultes
Indications | Posologie | Durée du traitement | |
Cryptococcose | - Traitement des méningites à cryptocoques. | Dose de charge : 400 mg le premier jour | Habituellement au moins 6 à 8 semaines. |
- Traitement d'entretien pour prévenir une rechute de méningite à cryptocoques chez les patients avec un risque élevé de rechute. | 200 mg une fois par jour | Durée indéterminée à une dose quotidienne de 200 mg. | |
Coccidioïdomycose | | 200 mg à 400 mg une fois par jour | 11 mois jusqu'à 24 mois ou plus, en fonction du patient. Une dose de 800 mg par jour peut être envisagée pour certaines infections et notamment en cas d'atteinte méningée. |
Candidose invasive |
| Dose de charge : 800 mg le premier jour | En règle générale, la durée recommandée du traitement de la candidémie est de 2 semaines après le premier résultat d'hémoculture négatif et après la résolution des signes et symptômes attribuables à la candidémie. |
Traitement de la candidose muqueuse | - Candidose oropharyngée | Dose de charge 200 mg à 400 mg le premier jour | 7 à 21 jours (jusqu’à la rémission de la candidose oropharyngée). |
- Candidose œsophagienne | Dose de charge 200 mg à 400 mg le premier jour | 14 à 30 jours (jusqu’à la rémission de la candidose œsophagienne). Des périodes plus longues peuvent être utilisées chez les patients sévèrement immunodéprimés. | |
- Candidurie | 200 mg à 400 mg une fois par jour | 7 à 21 jours. Des périodes plus longues peuvent être utilisées chez les patients sévèrement immunodéprimés. | |
- Candidose atrophique chronique | 50 mg une fois par jour | 14 jours. | |
- Candidose cutanéo-muqueuse chronique | 50 mg à 100 mg une fois par jour | Jusqu'à 28 jours. Périodes plus longues en fonction à la fois de la sévérité de l'infection ou de l'immunosuppression sous-jacente et de l'infection. | |
Prévention de récidive d'une candidose muqueuse chez les patients infectés par le VIH présentant un haut risque de récidive | - Candidose oropharyngée | 100 mg à 200 mg une fois par jour ou 200 mg 3 fois par semaine. | Période indéterminée chez les patients avec une immunosuppression chronique. |
- Candidose œsophagienne | 100 mg à 200 mg une fois par jour ou 200 mg 3 fois par semaine. | Période indéterminée chez les patients avec une immunosuppression chronique. | |
Candidose génitale | - Candidose vaginale aiguë | 150 mg | Dose unique. |
- Traitement et prophylaxie des candidoses vaginales récurrentes (4 épisodes ou plus par an). | 150 mg tous les 3 jours à raison de 3 doses au total (J1, J4 et J7), suivis d'une dose d'entretien de 150 mg une fois par semaine | Dose d'entretien : 6 mois. | |
Dermatomycose | - tinea pedis, | 150 mg une fois par semaine ou 50 mg une fois par jour | 2 à 4 semaines, tinea pedis peut nécessiter un traitement allant jusqu'à 6 semaines. |
- tinea versicolor | 300 mg à 400 mg une fois par semaine | 1 à 3 semaines. | |
50 mg une fois par jour | 2 à 4 semaines. | ||
- tinea unguium (onychomycose) | 150 mg une fois par semaine | Le traitement doit être poursuivi jusqu'au remplacement de l'ongle infecté (repousse d'un ongle non infecté). La repousse des ongles des doigts et des ongles des orteils nécessite normalement respectivement 3 à 6 mois et 6 à 12 mois. Les taux de croissance peuvent toutefois varier de manière importante entre individus et en fonction de l'âge. Après le succès du traitement d'infections chroniques de longue durée, les ongles peuvent occasionnellement rester déformés. | |
Prophylaxie des infections à Candida chez les patients atteints de neutropénie prolongée |
| 200 mg à 400 mg une fois par jour | Le traitement doit débuter plusieurs jours avant le début de la neutropénie induite et se poursuivre pendant 7 jours après la résolution de la neutropénie (taux de neutrophiles supérieur à 1000 cellules par mm3). |
Populations particulières
Sujets âgés :
La posologie devra être ajustée sur la base de la fonction rénale (voir « Insuffisance rénale »).
Insuffisance rénale :
Diflucan est principalement excrété dans les urines sous forme de substance active inchangée. Lors du traitement à dose unique, aucun ajustement de la posologie n'est nécessaire. Chez les patients (y compris les enfants) présentant une altération de la fonction rénale qui recevront des doses répétées de fluconazole, une dose initiale de 50 mg à 400 mg doit être administrée, en fonction de la posologie quotidienne recommandée dans l'indication concernée. Après cette dose de charge initiale, la dose quotidienne (selon l'indication) doit être ajustée selon le tableau suivant :
Clairance de la créatinine (ml/min) | Pourcentage de la dose recommandée |
> 50 | 100 % |
≤ 50 (pas d’hémodialyse) | 50 % |
Hémodialyse | 100 % après chaque hémodialyse |
Les patients en hémodialyse doivent recevoir 100 % de la dose recommandée après chaque hémodialyse ; les jours de non-dialyse, les patients doivent recevoir une dose réduite en fonction de leur clairance de la créatinine.
Insuffisance hépatique :
Les données disponibles chez les patients présentant une insuffisance hépatique sont limitées, le fluconazole doit donc être administré avec prudence chez les patients présentant une altération de la fonction hépatique (voir rubriques 4.4 et 4.8).
Population pédiatrique
Une posologie maximale de 400 mg par jour ne doit pas être dépassée dans la population pédiatrique.
Comme dans les infections similaires chez l'adulte, la durée du traitement est basée sur la réponse clinique et mycologique. Diflucan est administré en une prise unique quotidienne.
Chez les patients pédiatriques qui présentent une altération de la fonction rénale, voir la posologie à la rubrique “Insuffisance rénale”. La pharmacocinétique du fluconazole n'a pas été étudiée dans la population pédiatrique présentant une insuffisance rénale (pour les « nouveau-nés à terme » qui présentent souvent une immaturité rénale primaire, veuillez voir ci-dessous).
Nourrissons, jeunes enfants et enfants (âgés de 28 jours à 11 ans) :
Indication | Posologie | Recommandations |
- Candidose muqueuse | Dose initiale : 6 mg/kg | La dose initiale peut être utilisée le premier jour afin d'atteindre plus rapidement les taux à l'état d'équilibre |
- Candidose invasive | Dose : 6 à 12 mg/kg une fois par jour | En fonction de la sévérité de la maladie |
- Traitement d'entretien pour prévenir les rechutes de la méningite à cryptocoques chez les enfants présentant un risque élevé de rechute | Dose : 6 mg/kg une fois par jour | En fonction de la sévérité de la maladie |
- Prophylaxie des infections à Candida chez les patients immunodéprimés | Dose : 3 à 12 mg/kg une fois par jour | En fonction de l'importance et de la durée de la neutropénie induite (voir posologie chez l'adulte) |
Adolescents (âgés de 12 à 17 ans) :
Le prescripteur déterminera la posologie la plus appropriée (adultes ou enfants) en fonction du poids et du développement pubère de l'adolescent. Les données cliniques indiquent que les enfants ont une clairance du fluconazole plus élevée que celle observée chez les adultes. Une dose de 100, 200 et 400 mg chez l'adulte correspond à une dose de 3, 6 et 12 mg/kg chez l'enfant pour obtenir une exposition systémique comparable.
La sécurité et l'efficacité dans l’indication candidose génitale dans la population pédiatrique n'ont pas été établies. Les données de sécurité actuellement disponibles pour d’autres indications pédiatriques sont décrites à la rubrique 4.8. Si le traitement est impératif pour la candidose génitale chez les adolescents (de 12 à 17 ans), la posologie doit être la même que celle chez les adultes.
Nouveau-nés à terme (0 à 27 jours) :
Les nouveau-nés éliminent lentement le fluconazole.
On dispose de peu de données pharmacocinétiques à l'appui de cette posologie chez les nouveau-nés à terme (voir rubrique 5.2).
Groupe d'âge | Posologie | Recommandations |
Nouveau-nés à terme (0 à 14 jours) | La même dose en mg/kg que pour les nourrissons, jeunes enfants et enfants doit être administrée toutes les 72 heures | Une posologie maximale de 12 mg/kg toutes les 72 heures ne doit pas être dépassée |
Nouveau-nés à terme (âgés de | La même dose en mg/kg que pour les nourrissons, jeunes enfants et enfants doit être administrée toutes les 48 heures | Une posologie maximale de 12 mg/kg toutes les 48 heures ne doit pas être dépassée |
Mode d'administration
Diflucan peut être administré soit par voie orale (gélules, poudre pour suspension buvable et sirop) soit par perfusion intraveineuse (solution pour perfusion), la voie d'administration dépendant de l'état clinique du patient. Lors du passage de la voie intraveineuse à la voie orale, ou vice versa, il n'est pas nécessaire de modifier la dose quotidienne.
Le médecin doit prescrire la forme pharmaceutique et le dosage les plus appropriés en fonction de l’âge, du poids et de la dose. La formulation gélule n’est pas adaptée aux nourrissons et aux jeunes enfants. Des formulations orales liquides de fluconazole sont disponibles et mieux adaptées à cette population.
Diflucan peut être pris avec ou sans nourriture.
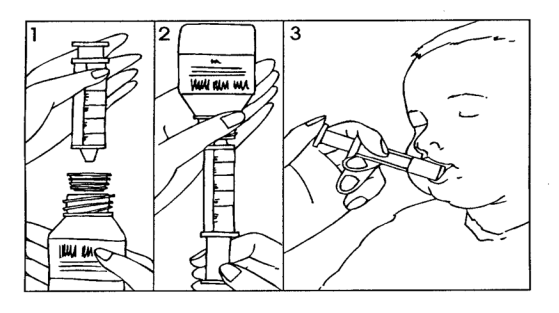
Pour les instructions concernant la reconstitution du médicament avant administration, voir rubrique 6.6. Après reconstitution, la suspension reconstituée sera une suspension blanche à blanc cassé au goût d'orange.
Pour une conversion de la posologie de la poudre pour la suspension buvable, de mg/ml en ml/kg de poids corporel (PC), chez les patients pédiatriques, voir rubrique 6.6.
Chez les patients adultes, calculer la dose à administrer en ml selon la posologie recommandée en mg et le dosage du produit.
4.3 Contre-indications
Hypersensibilité à la substance active, à d’autres dérives azolés, ou à l’un des excipients mentionnés à la rubrique 6.1.
L’association à la terfénadine est contre-indiquée chez les patients traités par Diflucan à doses répétées supérieures ou égales à 400 mg par jour sur la base des résultats d'une étude d'interaction à doses répétées. L’association avec d’autres médicaments connus pour prolonger l’intervalle QT et métabolisés par les cytochromes P450 (CYP) 3A4 tels que cisapride, astémizole, pimozide, quinidine et érythromycine est contre-indiquée chez les patients traités par fluconazole (voir rubriques 4.4 et 4.5).
4.8 Effets indésirables
Résumé du profil de sécurité
Une réaction médicamenteuse avec éosinophilie et symptômes systémiques (syndrome DRESS) a été rapportée en association avec un traitement par fluconazole (voir rubrique 4.4).
Les effets indésirables les plus fréquemment rapportés (≥ 1/100 à < 1/10) sont les céphalées, douleurs abdominales, diarrhées, nausées vomissements, augmentation de l’alanine aminotransférase, augmentation de l’aspartate aminotransférase, augmentation de la phosphatase alcaline sanguine et rash.
Les effets indésirables suivants ont été observés et rapportés durant le traitement par Diflucan avec les fréquences suivantes : Très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), peu fréquent (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000), très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Classes de systèmes d’organes | Fréquent | Peu fréquent | Rare | Fréquence indéterminée |
Affections hématologiques et du système lymphatique |
| Anémie | Agranulocytose, |
|
Affections du système immunitaire |
|
| Anaphylaxie |
|
Troubles du métabolisme et de la nutrition |
| Diminution de l’appétit | Hypercholestérolémie, |
|
Affections psychiatriques |
| Somnolence, |
|
|
Affections du système nerveux | Céphalées | Crises d’épilepsie, | Tremblements |
|
Affections de l’oreille et du labyrinthe |
| Vertiges |
|
|
Affections cardiaques |
|
| Torsade de pointes (voir rubrique 4.4), |
|
Affections gastro-intestinales | Douleurs abdominales, | Constipation, |
|
|
Affections hépatobiliaires | Augmentation de l’alanine aminotransférase (voir rubrique 4.4), | Cholestase (voir rubrique 4.4), | Insuffisance hépatique (voir rubrique 4.4), |
|
Affections de la peau et du tissu sous-cutané | Rash (voir rubrique 4.4) | Eruption médicamenteuse* (voir rubrique 4.4), | Syndrome de Lyell (nécrolyse épidermique toxique) (voir rubrique 4.4), | Réaction médicamenteuse avec éosinophilie et symptômes systémiques (syndrome DRESS) |
Affections musculo-squelettiques et systémiques |
| Myalgie |
|
|
Troubles généraux et anomalies au site d’administration |
| Fatigue, |
|
|
* y compris éruption fixe d’origine médicamenteuse
Population pédiatrique
La nature et l'incidence des effets indésirables et des anomalies biologiques observés pendant les essais cliniques pédiatriques, excluant l’indication dans la candidose génitale, sont comparables à celles observées chez l’adulte.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via :
Belgique : l’Agence fédérale des médicaments et des produits de santéwww.afmps.be - Division Vigilance :
Site internet: www.notifieruneffetindesirable.be
e mail: adr@afmps.be
Luxembourg : Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la SantéSite internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHÉ
Pfizer NV/SA, Boulevard de la Plaine 17, 1050 Bruxelles, Belgique.
8. NUMÉROS D’AUTORISATION DE MISE SUR LE MARCHÉ
Diflucan 10 mg/ml poudre pour suspension buvable, flacon de 60 ml : BE160422 ; LU2003097827
Diflucan 40 mg/ml poudre pour suspension buvable, flacon de 60 ml : BE160413 ; LU2003097828
10. DATE DE MISE À JOUR DU TEXTE
11/2024
24J01
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 1509355 | DIFLUCAN PULV PR SUSP 50MG/5ML | J02AC01 | € 13,17 | - | Oui | € 2 | € 1 |
| 1509363 | DIFLUCAN PULV PR SUSP 200MG/5ML | J02AC01 | € 30,04 | - | Oui | € 2 | € 1 |